Denne RNA-baserede teknik kunne gøre genterapi mere effektiv

Kredit:CC0 Public Domain
Levering af funktionelle gener til celler for at erstatte muterede gener, en metode kendt som genterapi, har potentiale til behandling af mange former for sygdomme. De tidligste bestræbelser på at levere gener til syge celler fokuserede på DNA, men mange videnskabsmænd undersøger nu muligheden for at bruge RNA i stedet, som kunne tilbyde forbedret sikkerhed og lettere levering.
MIT biologiske ingeniører har nu udtænkt en måde at regulere ekspressionen af RNA, når det kommer ind i celler, giver dem præcis kontrol over den dosis protein, som en patient modtager. Denne teknologi kunne give læger mulighed for mere præcist at skræddersy behandling til individuelle patienter, og det giver også en måde at hurtigt slukke generne på, Hvis det er nødvendigt.
"Vi kan meget diskret kontrollere, hvordan forskellige gener udtrykkes, "siger Jacob Becraft, en MIT -kandidatstuderende og en af undersøgelsens hovedforfattere, som optræder i 16. oktober-udgaven af Naturens kemiske biologi . "Historisk set genterapier har stødt på problemer med hensyn til sikkerhed, men med nye fremskridt inden for syntetisk biologi, vi kan skabe helt nye paradigmer for 'smarte terapeutika', der aktivt engagerer sig i patientens egne celler for at øge effektiviteten og sikkerheden."
Becraft og hans kolleger på MIT har startet en virksomhed for at videreudvikle denne tilgang, med indledende fokus på kræftbehandling. Tyler Wagner, en nylig Boston University Ph.D. modtager, er også hovedforfatter af papiret. Tasuku Kitada, en tidligere MIT postdoc, og Ron Weiss, en MIT -professor i biologisk teknik, er seniorforfattere.
RNA kredsløb
Kun få genterapier er hidtil blevet godkendt til human brug, men forskere arbejder på og tester nye genterapibehandlinger for sygdomme som seglcelleanæmi, hæmofili, og medfødt øjensygdom blandt mange andre.
Som et redskab til genterapi, DNA kan være svært at arbejde med. Når det bæres af syntetiske nanopartikler, partiklerne skal leveres til kernen, som kan være ineffektiv. Vira er meget mere effektive til DNA -levering; imidlertid, de kan være immunogene, svært, og dyrt at producere, og ofte integrerer deres DNA i cellens eget genom, begrænser deres anvendelighed i genetiske terapier.
Messenger RNA, eller mRNA, tilbyder en mere direkte, og ikke-permanent, måde at ændre cellernes genekspression på. I alle levende celler, mRNA bærer kopier af informationen indeholdt i DNA til celleorganeller kaldet ribosomer, som samler proteiner kodet af gener. Derfor, ved at levere mRNA, der koder for et bestemt gen, forskere kan inducere produktion af det ønskede protein uden at skulle få genetisk materiale ind i en celles kerne eller integrere det i genomet.
For at hjælpe med at gøre RNA-baseret genterapi mere effektiv, MIT-teamet satte sig for præcist at kontrollere produktionen af terapeutiske proteiner, når RNA'et kommer ind i cellerne. At gøre det, de besluttede at tilpasse syntetisk biologi principper, som muliggør præcis programmering af syntetiske DNA-kredsløb, til RNA.
Forskernes nye kredsløb består af en enkelt RNA-streng, der omfatter gener for de ønskede terapeutiske proteiner samt gener for RNA-bindende proteiner, som styrer ekspressionen af de terapeutiske proteiner.
"På grund af replikationens dynamiske natur, kredsløbets ydeevne kan indstilles, så forskellige proteiner kan udtrykkes på forskellige tidspunkter, alle fra den samme streng af RNA, " siger Becraft.
Dette gør det muligt for forskerne at tænde kredsløbene på det rigtige tidspunkt ved at bruge "små molekyler" lægemidler, der interagerer med RNA-bindende proteiner. Når et lægemiddel såsom doxycyclin, som allerede er FDA-godkendt, føjes til cellerne, det kan stabilisere eller destabilisere interaktionen mellem RNA og RNA-bindende proteiner, afhængig af hvordan kredsløbet er designet. Denne interaktion bestemmer, om proteinerne blokerer RNA -genekspression eller ej.
I en tidligere undersøgelse, forskerne viste også, at de kunne bygge cellespecificitet ind i deres kredsløb, så RNA'et kun bliver aktivt i målcellerne.
Målrettet mod kræft
Det firma, forskerne startede, Strand Therapeutics, arbejder nu på at tilpasse denne tilgang til cancerimmunterapi – en ny behandlingsstrategi, der involverer stimulering af en patients eget immunsystem til at angribe tumorer.
Ved hjælp af RNA, forskerne planlægger at udvikle kredsløb, der selektivt kan stimulere immunceller til at angribe tumorer, gør det muligt at målrette tumorceller, der har metastaseret til svært tilgængelige dele af kroppen. For eksempel, det har vist sig vanskeligt at målrette mod kræftceller, såsom lungelæsioner, med mRNA på grund af risikoen for at betyde lungevævet. Ved hjælp af RNA-kredsløb, forskerne leverer først deres terapi til målrettede kræftcelletyper i lungen, og gennem deres genetiske kredsløb, RNA'et ville aktivere T-celler, der kunne behandle kræftens metastaser andre steder i kroppen.
"Håbet er at fremkalde et immunrespons, som er i stand til at opfange og behandle resten af metastaser i hele kroppen, " siger Becraft. "Hvis du er i stand til at behandle et sted af kræften, så tager dit immunsystem sig af resten, fordi du nu har opbygget et immunrespons mod det. "
Ved at bruge denne slags RNA-kredsløb, læger ville være i stand til at justere doser baseret på, hvordan patienten reagerer, siger forskerne. Kredsløbene giver også en hurtig måde at slukke for terapeutisk proteinproduktion i tilfælde, hvor patientens immunsystem bliver overstimuleret, som kan være dødelig.
I fremtiden, forskerne håber at udvikle mere komplekse kredsløb, der kan være både diagnostiske og terapeutiske - først opdage et problem, såsom en tumor, og derefter producere det passende lægemiddel.
 Varme artikler
Varme artikler
-
 Forskere ser kemisk rækkevidde i mellem-entropi-legeringKredit:CC0 Public Domain Kinesiske forskere har foretaget direkte observationer af ansigtscentrerede kubiske VCoNi (medium) -entropylegeringer (MEA) og for første gang foreslået en overbevisende i
Forskere ser kemisk rækkevidde i mellem-entropi-legeringKredit:CC0 Public Domain Kinesiske forskere har foretaget direkte observationer af ansigtscentrerede kubiske VCoNi (medium) -entropylegeringer (MEA) og for første gang foreslået en overbevisende i -
 Kemikere skaber en ny vej til PHA'er:naturligt nedbrydeligt bioplastFra venstre:kandidatstuderende Andrea Westlie, professor Eugene Chen, og forsker Xiaoyan Tang i Chemistry Research Building. Kredit:John Eisele En bølge af offentlig fremdrift svulmer op mod krise
Kemikere skaber en ny vej til PHA'er:naturligt nedbrydeligt bioplastFra venstre:kandidatstuderende Andrea Westlie, professor Eugene Chen, og forsker Xiaoyan Tang i Chemistry Research Building. Kredit:John Eisele En bølge af offentlig fremdrift svulmer op mod krise -
 Små porøse krystaller ændrer vandets form for at fremskynde kemiske reaktionerKemiske og biomolekylære ingeniørforskere fra University of Illinois undersøgte, hvordan vandmolekyler samles og ændrer form for at afsløre strategier, der fremskynder kemiske reaktioner, der er kriti
Små porøse krystaller ændrer vandets form for at fremskynde kemiske reaktionerKemiske og biomolekylære ingeniørforskere fra University of Illinois undersøgte, hvordan vandmolekyler samles og ændrer form for at afsløre strategier, der fremskynder kemiske reaktioner, der er kriti -
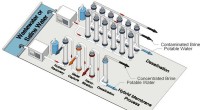 Membran kan bedre behandle spildevand, genvinde værdifulde ressourcerForskere foreslår, at nuværende afsaltningsprocesser og fremtidige hybride bruger en blokpolymermembran til at behandle ukonventionelle vandkilder. Kredit:University of Notre Dame billede/Yizhou Zhang
Membran kan bedre behandle spildevand, genvinde værdifulde ressourcerForskere foreslår, at nuværende afsaltningsprocesser og fremtidige hybride bruger en blokpolymermembran til at behandle ukonventionelle vandkilder. Kredit:University of Notre Dame billede/Yizhou Zhang
- Forskere afslører ny indsigt i kontrollen af cellulære stilladser
- Forskere udvikler homing beacon-lægemidler til at målrette mod kræftceller
- Forladte glasfiberbåde frigiver toksiner og mikroplast over hele verden
- THz-spektroskopi sporer elektronopløsning i fotoioniseret vand
- Team udvikler armbånd, der blokerer mikrofoner
- Facebook fornyer værktøjer til beskyttelse af personlige oplysninger, efterhånden som strammere E…


