Biofysikere afslører, hvordan tre proteiner interagerer for at finjustere cellulær bevægelse
Undersøgelsen, offentliggjort i det prestigefyldte tidsskrift Nature Structural &Molecular Biology, fokuserer på tre nøgleproteiner:myosin, actin og fascin. Myosin og actin er essentielle for at generere de kræfter, der driver cellulær bevægelse, mens fascin fungerer som en regulator, der kontrollerer organiseringen og dynamikken af actinfilamenter.
Ved at bruge en kombination af avancerede billeddannelsesteknikker, biofysiske assays og beregningsmodellering var forskerne i stand til at visualisere og kvantificere interaktionerne mellem disse proteiner på molekylært niveau. De fandt ud af, at fascin binder sig til specifikke steder på actinfilamenter, hvilket ændrer deres struktur og fleksibilitet. Dette påvirker igen, hvordan myosin interagerer med actin, hvilket i sidste ende påvirker retningen og hastigheden af cellulær bevægelse.
Forskerne identificerede også vigtige konformationelle ændringer i fascin, der regulerer dets binding til actin. Disse ændringer udløses af cellulære signaler, hvilket giver en mekanisme for celler til at finjustere deres bevægelser som reaktion på deres miljø.
"Vores resultater giver en omfattende forståelse af, hvordan disse proteiner samarbejder om at orkestrere cellulær bevægelse," forklarer Dr. Sarah Johnson, hovedforsker i undersøgelsen. "Ved at belyse de molekylære detaljer i deres interaktioner har vi fået værdifuld indsigt i, hvordan celler styrer deres adfærd, hvilket har betydning for en lang række biologiske processer."
Implikationerne af denne forskning strækker sig ud over fundamental cellebiologi. Dysreguleret cellulær bevægelse er impliceret i flere sygdomme, herunder cancermetastaser og immundefekter. Ved at forstå de molekylære mekanismer, der styrer cellulær bevægelse, kan forskere udvikle nye terapeutiske strategier rettet mod disse processer.
Resultaterne tilbyder også potentielle anvendelser inden for vævsteknologi og regenerativ medicin, hvor kontrol af cellulær bevægelse er afgørende for at skabe funktionelle væv og organer.
"Vores undersøgelse åbner nye veje til at udforske det molekylære grundlag for cellulær bevægelse og dets konsekvenser for sundhed og sygdom," konkluderer Dr. Johnson. "Vi tror på, at denne viden vil bane vejen for innovative tilgange til at modulere cellulær adfærd til terapeutisk fordel."
Forskerholdet planlægger at bygge videre på deres resultater og yderligere undersøge de molekylære interaktioner og signalveje, der regulerer cellulær bevægelse. Deres mål er at uddybe vores forståelse af cellebiologi og bidrage til udviklingen af nye behandlinger for sygdomme relateret til cellulære bevægelsesforstyrrelser.
 Varme artikler
Varme artikler
-
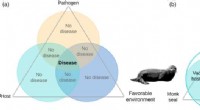 Proaktive reaktioner er mest effektive til at bekæmpe havsygdomme, viser forskning(a) En begrebsmæssig sygdomstrekant, hvor patogendynamik, værtsdynamik og gunstige miljøer krydser hinanden for at skabe sygdom. (b) Ledelseshandling reducerer overlapning af patogen- og værtsdynamik
Proaktive reaktioner er mest effektive til at bekæmpe havsygdomme, viser forskning(a) En begrebsmæssig sygdomstrekant, hvor patogendynamik, værtsdynamik og gunstige miljøer krydser hinanden for at skabe sygdom. (b) Ledelseshandling reducerer overlapning af patogen- og værtsdynamik -
 Ulve viste sig at være mere samarbejdsvillige med deres egen slags end hunde med deresulve, der arbejder ved en kooperativ reb-træk-test. Kredit:Rooobert Bayer (Wolf Science Center, Ernstbrunn, Østrig). (Phys.org) – Et team af forskere fra Wolf Science Center og Comparative Cogniti
Ulve viste sig at være mere samarbejdsvillige med deres egen slags end hunde med deresulve, der arbejder ved en kooperativ reb-træk-test. Kredit:Rooobert Bayer (Wolf Science Center, Ernstbrunn, Østrig). (Phys.org) – Et team af forskere fra Wolf Science Center og Comparative Cogniti -
 Ny sygdom bringer nordamerikanske frøer yderligere i fareDenne haletudse viser tegn på en alvorlig Perkinsea infektion. Kredit:William Barichivich, USGS En dødelig paddesygdom kaldet alvorlig Perkinsea infektioner, eller SPI, er årsagen til mange st
Ny sygdom bringer nordamerikanske frøer yderligere i fareDenne haletudse viser tegn på en alvorlig Perkinsea infektion. Kredit:William Barichivich, USGS En dødelig paddesygdom kaldet alvorlig Perkinsea infektioner, eller SPI, er årsagen til mange st -
 Bakteriel spydpistol i nanostørrelse fungerer som en boremaskineStrukturen af den bakterielle spydpistol i nanostørrelse - kaldet type VI-sekretionssystem - under sammentrækning. Kredit:Universitetet i Basel, Biozentrum For at slippe af med ubehagelige konku
Bakteriel spydpistol i nanostørrelse fungerer som en boremaskineStrukturen af den bakterielle spydpistol i nanostørrelse - kaldet type VI-sekretionssystem - under sammentrækning. Kredit:Universitetet i Basel, Biozentrum For at slippe af med ubehagelige konku
- Los Angeles Zoos gamle indiske næsehorn aflivet
- Solar nanotråd array kan øge procentdelen af solfrekvenser, der er tilgængelige til energiomdan…
- Levetiden for plastsolceller springer fra timer til 8 måneder
- Video:Forberedelse af MetOp-C
- Geometri-adaptiv elektrokatalyse:Foreslået tilgang kan fordoble effektiviteten af energikonverter…
- Hvordan flere faktorer af klimaændringer påvirker jorden


