At se mindre gennemgående celler:En naturlig enkeltcellet biomagnifier til billedbehandling med subbølgelængde
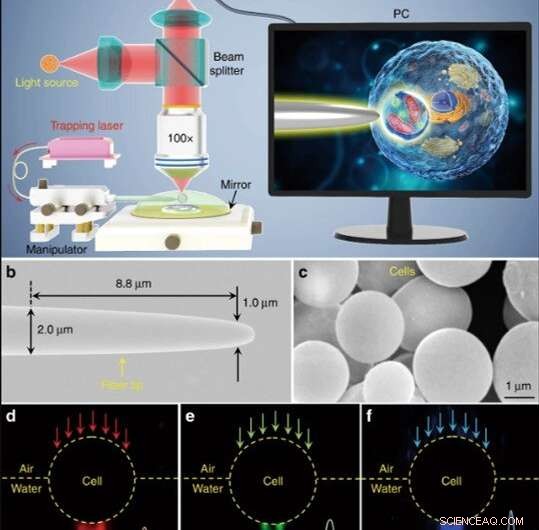
Skematisk illustration og materiel karakterisering. (a) Skematisk illustration af den eksperimentelle opsætning. Et konventionelt refleksionsmodusmikroskop udstyret med et CCD-kamera og × 100 objektiv blev brugt til at observere prøver og optage billeder. Indsatsen vist på en pc -skærm, der skematisk viser, hvordan biomagnifikatoren bruges til at forstørre og afbilde de subcellulære strukturer inde i en bioprøve. (b) SEM -billede af fiberspidsen med en diameter på 1,0 um i dens koniske ende. (c) SEM-billede, der viser gærcellebaserede bioforstørrere med glatte overflader og sfæriske former. d-f Mørkefeltbilleder, der viser 644 nm rødt lys (d), 532 nm grønt lys (e), og 473 nm blåt lys (f), der transmitterer gennem biomagnifikatoren og fokuseres på lyspunkter med subbølgelængde med taljeradier på 370, 300, og 270 nm, henholdsvis. Kredit:Light:Science &Applications, doi:10.1038/s41377-019-0168-4
Optiske mikroskoper og pincetter kan afbilde og manipulere objekter i mikroskalaen til applikationer inden for cellulær og molekylær biologi. Den optiske opløsning er, imidlertid, hæmmet af diffraktionsgrænsen, og derfor er både mikroskoper og pincet ikke i stand til direkte at billede og manipulere nano-objekter. Nye teknikker i plasmoniske/fotoniske nanoskoper og nanotweezere har til formål at opnå nanometer-opløsning, selvom materialestrukturer med højt indeks let kan forårsage mekaniske og fototermiske skader på nanoskala biospecimener.
I en nylig undersøgelse nu offentliggjort den Lys:Videnskab og applikationer , Yuchao Li og kolleger ved Institute of Nanophotonics i Kina, udviklet et optisk mikroskop system ved hjælp af levende celler som bittesmå linser til billede og manipulere objekter mindre end lysets bølgelængde. De viste sub-diffraktionsgrænse billeddannelse og manipulation af nano-objekter med en ikke-invasiv enhed, som de konstruerede ved at fange en celle på en fiberspids. Den fangede celle dannede en biomagnifier, der kunne forstørre nanostrukturer med en opløsning på 100 nm, under hvidt lysmikroskopi. Ved hjælp af biomagnifier, Li et al. dannet en nano-optisk fælde til præcist at manipulere en individuel nanopartikel med en radius på 50 nm. Teknikken giver et værktøj med høj præcision til optisk billeddannelse, registrering og samling af bio-nanomaterialer uden mekanisk eller fototermisk skade.
Optisk billeddannelse til manipulation af små objekter er afgørende for medicinsk diagnose, biologisk sansning, cellulær efterforskning, molekylær træning og materialemontering. Pincet og mikroskoper er standardudstyr til billedbehandling uden kontakt og manipulation af minutprøver, der spænder fra få nanometer til flere mikrometer. Alligevel, det er udfordrende at bruge teknologien til at tage billeder i nanoskala, da optisk opløsning er begrænset til cirka halvdelen af belysningsbølgelængden.
Forskere har opnået dramatiske fremskridt inden for nærfeltnanoskoper og nanotweezere i de sidste par årtier for at opnå optisk billeddannelse ved nanometeropløsning. Disse billeddannelsesteknikker blev tilbageholdt af uorganiske materialer med højt indeks, såsom ædelmetaller og halvledere, der blev brugt til deres fremstilling-som mekanisk kan beskadige prøver af biologiske celler eller væv under nærfeltbilleddannelse og manipulation.
Forskere undersøgte derfor enklere optiske billeddannelsesordninger baseret på dielektriske mikrosfærer for at overvinde den diffraktionsgrænse, der er almindelig for konventionelle mikroskoper. Selvom teknikken er etiketfri og mulig, sådanne mikrosfærer er baseret på kunstige uorganiske materialer, såsom siliciumdioxid (SiO 2 ), titandioxid (TiO 2 ) og bariumtitanat (BaTiO 3 ). Forskere er derfor interesserede i at udvikle et naturligt biomateriale til at konstruere en biokompatibel enhed til bioimaging, manipulation og biomagnificering ved nanoskala rumlig opløsning.
(a) Skematisk illustration af den eksperimentelle opsætning. Et konventionelt refleksionsmodusmikroskop udstyret med et CCD-kamera og × 100 objektiv blev brugt til at observere prøver og optage billeder. Indsatsen vist på en pc -skærm, der skematisk viser, hvordan biomagnifikatoren bruges til at forstørre og afbilde de subcellulære strukturer inde i en bioprøve. Kredit:Light:Science &Applications, doi:10.1038/s41377-019-0168-4 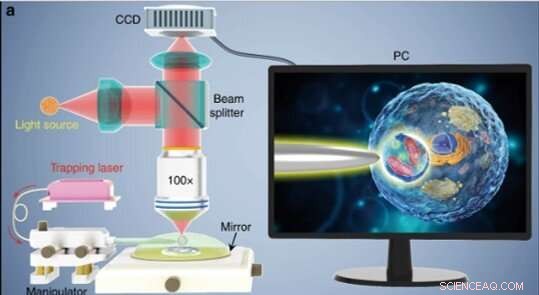
Forskerne udførte alle eksperimenter under et optisk mikroskop med refleksionsmåde koblet til et ladningskoblet enhed (CCD) kamera og objektiv. De brugte lyskilder ved 390 nm, 560 nm og 808 nm til excitation, henholdsvis belysning og fangst. Ved hjælp af en optisk fiber med en konisk spids, Li et al. fanget biomagnifier i enden af fiberen, som de kontrollerede ved at flytte spidsen ved hjælp af en mikromanipulator. Li et al. udvalgte glatte og sfæriske celler for at minimere billedafvigelse og bemærkede, at cellerne udviser bedre fokuseringsevne, når de er halvdypede i opløsning for at opretholde cellelevedygtighed.
Eksperimentel billeddannelse af forskellige biomagnificatorer. (a) Skematisk diagram, der viser, at biomagnifikatoren indsamler nærfelt nanostrukturer fra et objekt og danner et praktisk talt forstørret billede, der kan fanges af et konventionelt optisk mikroskop. (b – e) Optiske billeder af forskellige biomagnificatorer konstrueret af bakteriel (b), gær (c), rødt blod (d), og stamceller (e), der er delvist nedsænket i cellesuspension. f SEM-billede af et todimensionalt sekskantet tætpakket silica-nanosfærearray, der er samlet ved hjælp af en fotophereseteknik. (g – j) Optiske billeder af silica -nanosfærearrayet forstørret gennem bioforstørrere baseret på bakteriel (g), gær (h), rødt blod (i), og stamceller (j). (k) SEM-billede af overfladen på et Blu-ray-gitter med en linjebredde på 200 nm og mellemrum på 100 nm. l – o Optiske billeder af Blu-ray-gitterstrukturen forstørret gennem bioforstørrere baseret på bakteriel (l), gær (m), rødt blod (n), og stamceller (o). p Intensitetsprofil langs den stiplede linje på tværs af Blu-ray-gitterstrukturen angivet i o. q Blå prikker, der viser forstørrelsesfaktoren M for de billeder, som biomagnifikatorerne får som en funktion af biomagnifier -diameteren. Kredit:Light:Science &Applications, doi:10.1038/s41377-019-0168-4 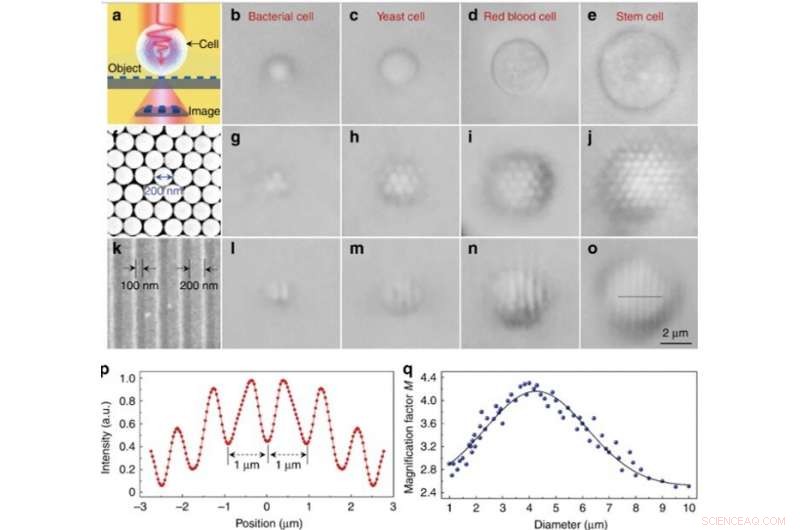
Kun nanosfærer med biomagnificatorer oven på dem kunne løses under billeddannelse, der henviser til, at nanosfærer uden bioforstørrere ikke kunne løses ved hjælp af et konventionelt mikroskop. Forstørrelsesfaktoren M for stamcellebaserede bioforstørrere blev bestemt til at være 3,3 gange større (x3,3), og forskerne viste, at den eksperimentelle M var afhængig af biomagnifierens diameter. Efterfølgende, Li et al. udførte alle eksperimenter ved hjælp af bioforstørrere med denne diameter.
Nano-optisk billeddannelse af subcellulære strukturer og nanopatronerede bogstaver. (en, b) Optiske billeder af subcellulære strukturer i en human epitelcelle ved hjælp af et konventionelt optisk mikroskop (a) og bioforstørrere (b). Positionerne for fire bioforstørrere er markeret som A – D. Til sammenligning, bioforstørrere kan løse det fibrøse cytoskelet (angivet som A – C) inde i cellen og to-lags strukturer (angivet som D) på cellemembranen, som ikke kan skelnes med det konventionelle mikroskop. c – e SEM (c), mørkt felt (d), og optiske billeder (e) af nanopatronede bogstaver JNU, der repræsenterer akronymet for Jinan University. Linjebredden af de nanopatternede bogstaver er 100 nm, som er mindre end diffraktionsgrænseopløsningen for det konventionelle optiske mikroskop. f – h Optiske billeder, der viser, at biomagnifikatoren fanget på fiberspidsen kan scanne og afbilde de nanopatruterede bogstaver J (f), N (g), og U (h) ved at flytte fiberen. Linjebredden af de nanopatronede bogstaver blev forstørret fra 100 til 400 nm. Kredit:Light:Science &Applications, doi:10.1038/s41377-019-0168-4 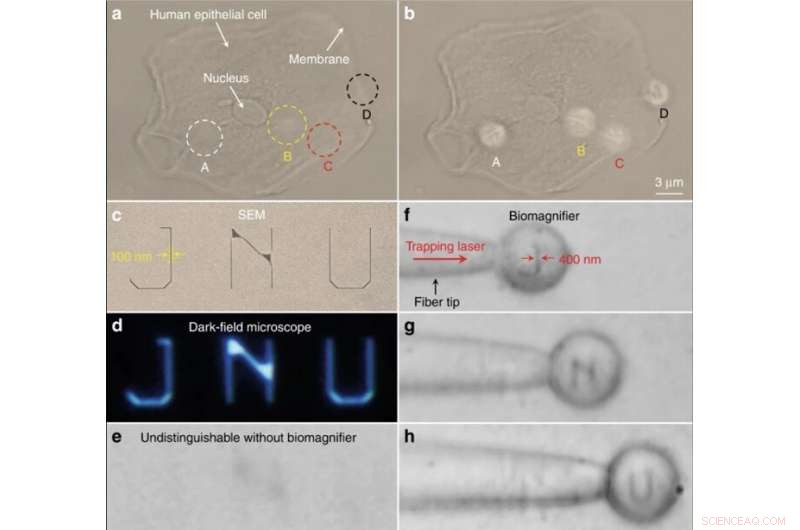
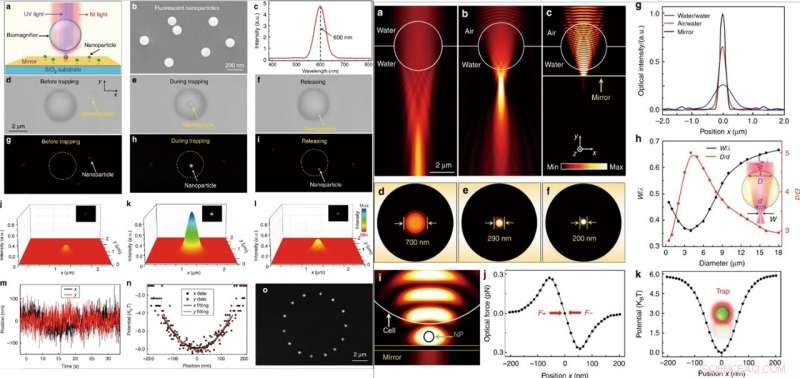
VENSTRE:Optisk manipulation af en enkelt fluorescerende nanopartikel. (a) Skematisk diagram, der viser en fluorescerende nanopartikel suspenderet på overfladen af et spejl og fanget af biomagnifier. (b) SEM -billede, der viser PS -fluorescerende nanopartikler med en gennemsnitlig radius på 50 nm. (c) Emissionsspektrum, der viser den centrale emissionsbølgelængde for de fluorescerende nanopartikler placeret ved 600 nm. (d – f) Optiske billeder viser fangstprocessen for en enkelt PS -nanopartikel med biomagnifikatoren. Processen bestod af tre på hinanden følgende trin:før indfangning (d), under fangst (e), og efter frigivelse (f). g – i Fluorescensbilleder, der viser fluorescensstedet på PS -nanopartiklen, før de bliver fanget (g), under fangst (h), og efter frigivelse (i). j – l Tredimensionel farvekortlægning af nanopartiklens fluorescenspletter som vist i g – i. m Spor i realtid af placeringen af den fangede nanopartikel i x- og y-retningerne. (n) Fangspotentiale for den fangede nanopartikel i x- og y -retninger med parabelbeslag. (o) Sammensatte fluorescensbilleder viser bevægelsessporet for den fangede nanopartikel i x -y -planet ved kontrolleret bevægelse af biomagnifikatoren. HØJRE:Numerisk simulering og beregning. (a – c) Optiske intensitetsfordelinger af lys med fokus på en 4 µm biomagnifier, der er fuldstændig nedsænket i vand (a), halvt nedsænket i vand (b), og ophængt på overfladen af et spejl (c). Belysningslyskilden blev indstillet som en gaussisk stråle med en bølgelængde på 560 nm. (d – f) Optiske intensitetsfordelinger af lyspunkterne fra biomagnifikatoren svarende til (a – c) i x – z -planet. (g) Optiske intensitetsprofiler ved brændplanerne for udgangslyset fra biomagnifikatorerne i x -retningen. (h) FEM -simuleringsresultater for den normaliserede talje af lyspunktet w/λ (w er lyspunktets taljeradius og λ er indgangslysets bølgelængde) og forholdet D/d (bredden af det lineære område hvor lys kommer ind i biomagnifier på dens forside kaldes D, og bredden af den udgående lysstråle på den bageste overflade er (d) som en funktion af biomagnifier -diameteren. (i) Simuleret intensitetsfordeling af nær-infrarødt fangstlys, der viser, at en nanopartikel (radius:50 nm) er fanget i kløften mellem biomagnifier og spejl. Den optiske inputeffekt for indfangningslyset blev indstillet til 10 mW. (j) Simulerede optiske kræfter i nanopartiklen fanget i lyspunktet som en funktion af nanopartikelpositionen langs x -retningen. (k) Beregnet fangstpotentiale for den fangede nanopartikel som en funktion af positionen langs x -retningen. Kredit:Light:Science &Applications, doi:10.1038/s41377-019-0168-4
Derefter, når de samtidig bestråler nær infrarøde (IR) og UV -laserstråler på biomagnifikatoren gennem en objektiv, de kunne fange og begejstre nanopartiklerne. Til disse forsøg, forskerne brugte fluorescerende nanopartikler med en gennemsnitlig radius på 50 nm. Da de fangede en enkelt nanopartikel i fokus for en biomagnifier, de observerede både optiske og fluorescerende billeder af prøven af interesse. Li et al. derefter beregnet fældestivheden af partiklen i realtid ved hjælp af standard optisk pincet. Evnen til at manipulere en enkelt nanopartikel uden kontakt og præcist via optik vil være nyttig til at samle velregulerede nanostrukturer. Da Li et al. numerisk undersøgt billeddannelsesmekanismen og fangststivhed af bioforstørrere ved hjælp af 3D-simulering og COMSOL-software. De observerede subdiffraktionsgrænsen for lysfokusering som følge af en kombineret "fotonisk nanojet" -effekt og sammenhængende interferensforbedring af spejlet.
Begrænsninger af metoden omfattede billeddannelse aberration og forvrængning på grund af de inhomogene intracellulære strukturer i den naturlige biomagnifier, sammenlignet med dielektriske mikrosfærer med ensartede brydningsindekser. Heldigvis, intracellulære materialer var optisk gennemsigtige for synligt og nær-infrarødt lys, og de optiske interaktioner var relativt svage inde i en enkelt celle. Intracellulære aktiviteter kan også ændre den delvise brydningsindeksfordeling i en celle for at forårsage lysforvrængning under fangst og billeddannelse, men de fleste intracellulære aktiviteter var ultrahurtige og påvirkede ikke billeddannelsesordningen.
På denne måde, Yuchao Li og kolleger udviklede en ny eksperimentel billeddannelsesteknik og verificerede de eksperimentelle muligheder med FEM -simuleringer. Li et al. integrerede optiske nanoskoper og nanotweezere i en enkelt enhed til billedbehandling og manipulation af nanostrukturer samtidigt for første gang i det nuværende arbejde. De fremmede opløsningen af teknikken til 100 nm og foreslog en etiketfri billeddannelsesprocedure. Forskerne forestiller sig den levende biomagnifier for at åbne nye muligheder inden for superopløsende billeddannelse, realtidsføling og præcis nano-samling af bionanomaterialer til dannelse af nanoarchitectures af interesse.
© 2019 Science X Network
 Varme artikler
Varme artikler
-
 Fysikere narrer fotoner til at opføre sig som elektroner ved hjælp af et syntetisk magnetfeltStramning af en honeycomb-metasurface genererer et kunstigt magnetfelt for lys, som kan tunes ved at indlejre metasurfacen inde i en hulrumsbølgeleder. Kredit:University of Exeter Forskere har opd
Fysikere narrer fotoner til at opføre sig som elektroner ved hjælp af et syntetisk magnetfeltStramning af en honeycomb-metasurface genererer et kunstigt magnetfelt for lys, som kan tunes ved at indlejre metasurfacen inde i en hulrumsbølgeleder. Kredit:University of Exeter Forskere har opd -
 Quark-gluon plasma flyder som vand, ifølge ny undersøgelseKredit:CC0 Public Domain Hvad har kvark-gluonplasma - den varme suppe af elementarpartikler dannet få mikrosekunder efter Big Bang - til fælles med postevand? Forskere siger, at det er den måde, d
Quark-gluon plasma flyder som vand, ifølge ny undersøgelseKredit:CC0 Public Domain Hvad har kvark-gluonplasma - den varme suppe af elementarpartikler dannet få mikrosekunder efter Big Bang - til fælles med postevand? Forskere siger, at det er den måde, d -
 Nem videnskabelige opfindelser for børnBørn opfinder ofte ting uden at indse det. Nysgerrighed i hvordan tingene virker, og hvordan man bruger dem forskelligt, kombineret med barndoms fantasi, kan danne grundlag for store opfindelser. Vide
Nem videnskabelige opfindelser for børnBørn opfinder ofte ting uden at indse det. Nysgerrighed i hvordan tingene virker, og hvordan man bruger dem forskelligt, kombineret med barndoms fantasi, kan danne grundlag for store opfindelser. Vide -
 Forskere kortlægger den hemmelige bevægelse af kvantepartiklerKredit:Robert Couse-Baker Forskere fra University of Cambridge har kigget ind i kvantemekanikkens hemmelige område. I et teoretisk oplæg offentliggjort i tidsskriftet Fysisk gennemgang A , de ha
Forskere kortlægger den hemmelige bevægelse af kvantepartiklerKredit:Robert Couse-Baker Forskere fra University of Cambridge har kigget ind i kvantemekanikkens hemmelige område. I et teoretisk oplæg offentliggjort i tidsskriftet Fysisk gennemgang A , de ha
- Undersøgelse:Befolkninger af vidt udbredte træarter reagerer forskelligt på klimaændringer
- Hvor meget land er der behov for vindmøller?
- Meget effektiv charge-to-spin interkonvertering i grafen heterostrukturer
- Kemiske reaktioner, der skyldes farveændring
- Nyt materiale kan spare tid og penge inden for medicinsk billeddannelse og miljøsanering
- Bakteriefabrikker bruges til at opdage potentielle nye malariamedicin


