Hvad hvis protonen har et andet antal nuetroner?
* Protoner definerer elementet: Antallet af protoner i et atoms kerne bestemmer, hvilket element det er. For eksempel har alle hydrogenatomer et proton, alle heliumatomer har to protoner og så videre. Dette er grundlaget for den periodiske tabel.
* neutroner påvirker isotopen: Antallet af neutroner i et atom kan variere, selv inden for det samme element. Disse variationer kaldes isotoper .
* For eksempel har carbon-12 6 protoner og 6 neutroner, mens carbon-14 har 6 protoner og 8 neutroner.
* Isotoper af det samme element har de samme kemiske egenskaber (de opfører sig på samme måde i kemiske reaktioner), men kan have forskellige fysiske egenskaber (som masse og radioaktivitet).
* Ændring af antallet af protoner ændrer elementet: Hvis du skulle ændre antallet af protoner i en kerne, ville du grundlæggende ændre, hvilket element du ser på.
hvad hvis en proton havde et andet antal neutroner?
Dette spørgsmål er vanskeligt, fordi protoner er * defineret * som ikke har nogen neutroner. De er grundlæggende partikler, ikke sammensat af mindre dele.
* hypotetisk scenarie: Hvis vi kunne forestille os et scenarie, hvor en proton på en eller anden måde fik eller mistede neutroner, ville vi have at gøre med noget helt andet.
* En proton med yderligere neutroner ville ikke længere være en proton; Det ville være en ny, tungere og potentielt ustabil partikel.
* En proton, der mister neutroner, ville være endnu fremmed, da det så ville mangle en grundlæggende del af dens definition.
Key Takeaway: Antallet af neutroner er en vigtig del af forståelsen af isotoper, men det ændrer ikke den grundlæggende identitet af et element som bestemt af antallet af protoner.
Sidste artikelHvilken indflydelse har kanteffekt på elektriske felter?
Næste artikelHvad er Mazda 13b skaft rotationsretning?
 Varme artikler
Varme artikler
-
 Uhyggelige kvantepartikelpar flyver som underlige kurvekuglerI en uge, 900 processorer kørte parallelt for at beregne mulige flyvemønstre for par af kvantepartikler kaldet fermioner til en ny teoretisk fysikundersøgelse af ultrakoldt stof. Hovedefterforsker Uzi
Uhyggelige kvantepartikelpar flyver som underlige kurvekuglerI en uge, 900 processorer kørte parallelt for at beregne mulige flyvemønstre for par af kvantepartikler kaldet fermioner til en ny teoretisk fysikundersøgelse af ultrakoldt stof. Hovedefterforsker Uzi -
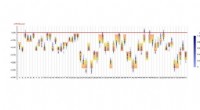 Fysikere demonstrerer ny måde at krænke lokal kausalitetDiagram over 61 værdier for overtrædelse af Bell ulighed. Kredit:Carvacho et al. Naturkommunikation (Phys.org)—For første gang, fysikere har eksperimentelt demonstreret krænkelsen af bilokal k
Fysikere demonstrerer ny måde at krænke lokal kausalitetDiagram over 61 værdier for overtrædelse af Bell ulighed. Kredit:Carvacho et al. Naturkommunikation (Phys.org)—For første gang, fysikere har eksperimentelt demonstreret krænkelsen af bilokal k -
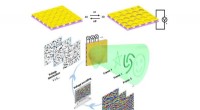 Rekonfigurerbare metaoverflader giver lysstyring i nanoskalaForskere designede rekonfigurerbare metaoverflader med 2D-spiraler, der deformeres, når en spænding påføres. Hver af spiralenhederne fungerer som en pixel og kan manipuleres uafhængigt. Forskerne demo
Rekonfigurerbare metaoverflader giver lysstyring i nanoskalaForskere designede rekonfigurerbare metaoverflader med 2D-spiraler, der deformeres, når en spænding påføres. Hver af spiralenhederne fungerer som en pixel og kan manipuleres uafhængigt. Forskerne demo -
 Følg ICARUS neutrinodetektorens fantastiske rejseICARUS-detektoren, set her i et renrum på CERN, er ved at blive forberedt på sin rejse til Fermilab. Kredit:CERN Den har levet i to forskellige lande, og det er ved at komme til en tredje. Det er
Følg ICARUS neutrinodetektorens fantastiske rejseICARUS-detektoren, set her i et renrum på CERN, er ved at blive forberedt på sin rejse til Fermilab. Kredit:CERN Den har levet i to forskellige lande, og det er ved at komme til en tredje. Det er
- Ny Grækenland brand bryder ud, foranlediger evakueringer
- Kvanteberegning:Kolde chips kan styre qubits
- Trump træder ind i sikkerhedsboble; vil han tage sin telefon med?
- Nyt katalysatormateriale producerer rigeligt billigt brint
- En moderator bruges i atomreaktorordre til?
- Hvad er eksempler på ikke-væske?


