Hvem sagde, at elektroner rejser i bestemte stier?
Bohr -modellen foreslog, at elektroner kredserer kernen på specifikke, cirkulære stier, ligesom planeter, der kredser om solen. Imidlertid blev denne model senere erstattet af kvantemekanisk model , som er en meget mere nøjagtig repræsentation af atomstruktur.
Den kvantemekaniske model Beskriver elektroner, der ikke er så små partikler, der kredser om kernen, men som sandsynlighedsbølger der findes i en skylignende region omkring kernen kaldet en orbital .
Dette betyder det:
* vi kan ikke forudsige den nøjagtige sti for en elektron. Vi kan kun beregne sandsynligheden for at finde et elektron i en bestemt region omkring kernen.
* elektroner følger ikke definerede stier. De findes som bølger, og deres opførsel styres af principperne for kvantemekanik.
Derfor er det forkert at sige, at elektroner rejser i bestemte stier. Ideen om definerede stier til elektroner er et forældet koncept fra en forenklet model af atomet.
Sidste artikelHvad er ligningen for Newtons anden lov?
Næste artikelHvor mange grader Celsius er 98 Fahrenheit?
 Varme artikler
Varme artikler
-
 LLNL-udviklet Petawatt-laser installeret på ELI BeamlinesL3-HAPLS lasersystem, installeret på ELI Beamlines Research Center i Dolní Břežany, Tjekkiet. Kredit:Lawrence Livermore National Laboratory L3-HAPLS avanceret petawatt-lasersystem blev installeret
LLNL-udviklet Petawatt-laser installeret på ELI BeamlinesL3-HAPLS lasersystem, installeret på ELI Beamlines Research Center i Dolní Břežany, Tjekkiet. Kredit:Lawrence Livermore National Laboratory L3-HAPLS avanceret petawatt-lasersystem blev installeret -
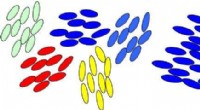 Forskning afslører, hvordan orden først opstår i flydende krystallerMolekyler i flydende krystaller går fra et uordnet virvar til mere ordnet justering med ændringer i temperatur. Men der er tegn på en mellemtilstand (venstre), hvor orden begynder at dukke op i diskre
Forskning afslører, hvordan orden først opstår i flydende krystallerMolekyler i flydende krystaller går fra et uordnet virvar til mere ordnet justering med ændringer i temperatur. Men der er tegn på en mellemtilstand (venstre), hvor orden begynder at dukke op i diskre -
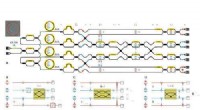 Første chip-til-chip kvanteteleportation, der udnytter silicon fotonisk chipfremstillingA. Chip Skematisk. Sorte linjer repræsenterer single mode bølgeledere for de enkelte fotoner, røde og blå pulser repræsenterer fotonenergien i hver vej. Gule bjælker repræsenterer ekstern fasekontrol.
Første chip-til-chip kvanteteleportation, der udnytter silicon fotonisk chipfremstillingA. Chip Skematisk. Sorte linjer repræsenterer single mode bølgeledere for de enkelte fotoner, røde og blå pulser repræsenterer fotonenergien i hver vej. Gule bjælker repræsenterer ekstern fasekontrol. -
 Nanotråde erstatter Newtons berømte glasprismeKredit:CC0 Public Domain Forskere har designet en ultra-miniaturiseret enhed, der direkte kan forestille enkeltceller uden behov for et mikroskop eller muliggøre kemisk fingeraftryksanalyse fra en
Nanotråde erstatter Newtons berømte glasprismeKredit:CC0 Public Domain Forskere har designet en ultra-miniaturiseret enhed, der direkte kan forestille enkeltceller uden behov for et mikroskop eller muliggøre kemisk fingeraftryksanalyse fra en
- Lås op for opskriften på magnetiske designerpartikler til næste generation af computerteknologier
- Google Maps til iOS giver dig nu mulighed for at dele opdateringer i realtid med venner
- Større, dyrere iPhone vist ved Apple -arrangement onsdag
- Forskere afslører unikke egenskaber ved en lovende ny superleder
- Mystiske skyabsorbere, der ses at drive venusisk albedo, klima
- Hvilket diagram repræsenterer aflejring?


