Hvad eksperimenterede J. Thomson med?
eksperimentet:
* katode strålerør: Thomson brugte et specialiseret glasrør kaldet et katodestrålerør (CRT). Dette rør blev evakueret (næsten al luft blev fjernet) og havde en højspænding påført på tværs af det.
* katodestråler: Når spændingen blev påført, blev en strøm af usynlige partikler, kendt som katodestråler, udsendt fra den negative elektrode (katode).
* magnetiske og elektriske felter: Thomson placerede magnetiske og elektriske felter omkring CRT. Han observerede, at katodestrålerne blev afbøjet af begge felter.
* Måling og analyse: Ved omhyggeligt at måle afbøjningen af strålerne i markerne var Thomson i stand til at bestemme ladning-til-masse-forholdet (E/M) for partiklerne.
* Opdagelse af elektronet: Thomsons beregninger viste, at partiklernes ladning og masse-forhold i katodestrålerne var meget højere end nogen kendt ion. Dette førte til, at han konkluderede, at katodestrålerne var sammensat af tidligere ukendte, negativt ladede partikler, som han kaldte elektroner .
Betydning af eksperimentet:
* atomstruktur: Thomsons eksperiment revolutionerede vores forståelse af atomet. Det viste, at atomer ikke er udelelige, men indeholder mindre, grundlæggende partikler.
* Elektronopdagelse: Hans opdagelse af elektronet banede vejen for yderligere forskning i stofstrukturen og udviklingen af kvantemekanik.
"Plum Pudding Model":
Baseret på hans eksperiment foreslog Thomson en model af atomet kaldet blomme budding -modellen . Denne model forestillede sig atomet som en sfære med positiv ladning med negativt ladede elektroner indlejret i den, som blommer i en budding. Mens denne model senere blev bevist forkert, var det et betydeligt skridt i forståelsen af atomstruktur.
 Varme artikler
Varme artikler
-
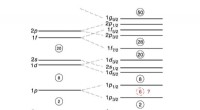 Forskere opdager hemmeligheden bag stabiliteten af kulstofisotoperFigur 1. Nukleare skalstrukturer for (til venstre) et radial afhængighedspotentiale (harmonisk oscillator) plus et lille kredsløbsvinkelmomentled, og (højre) med en ekstra spin-kredsløbskoblingskraft.
Forskere opdager hemmeligheden bag stabiliteten af kulstofisotoperFigur 1. Nukleare skalstrukturer for (til venstre) et radial afhængighedspotentiale (harmonisk oscillator) plus et lille kredsløbsvinkelmomentled, og (højre) med en ekstra spin-kredsløbskoblingskraft. -
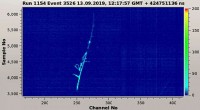 Test starter ved CERN for storstilet prototype af ny teknologi til at detektere neutrinoerDette billede viser et spor lavet af en kosmisk stråle-muon observeret i den tofasede ProtoDUNE-detektor. Den ionisering, der frigives af muonsporet i flydende argon og af den korrelerede elektromagne
Test starter ved CERN for storstilet prototype af ny teknologi til at detektere neutrinoerDette billede viser et spor lavet af en kosmisk stråle-muon observeret i den tofasede ProtoDUNE-detektor. Den ionisering, der frigives af muonsporet i flydende argon og af den korrelerede elektromagne -
 Smart timing får computere til at producere mindre varme - selv under Landauers grænseComputeroperationer, der producerer varme, påvirker også andre dele af kredsløbet. Ved hjælp af smart timing, energiomkostningerne kan reduceres. Kredit:University of Twente Computersystemer produ
Smart timing får computere til at producere mindre varme - selv under Landauers grænseComputeroperationer, der producerer varme, påvirker også andre dele af kredsløbet. Ved hjælp af smart timing, energiomkostningerne kan reduceres. Kredit:University of Twente Computersystemer produ -
 Spiralformet bevægelse i et granulært medium af en sandrobotKredit:University of Santiago At bevæge sig inden for granulære medier som sand er et trick, der ikke kun forekommer i science fiction-film. Sandfisk firben, som bor i ørkenen, er også i stand til
Spiralformet bevægelse i et granulært medium af en sandrobotKredit:University of Santiago At bevæge sig inden for granulære medier som sand er et trick, der ikke kun forekommer i science fiction-film. Sandfisk firben, som bor i ørkenen, er også i stand til
- Busser kvarts med en dråbe saltsyre?
- Paradigmeskift er nødvendigt for at designe tsunami-resistente broer
- Ny analyse af gamle fisk kan forklare, hvordan skulderen udviklede sig
- Konstruerede sandstænger måler ikke reder
- Opgradering af biomasse med selektive overflademodificerede katalysatorer
- Ingen planeter nødvendige:NASA-undersøgelse viser, at diskmønstre kan generere sig selv


