Hvad er formålet med Earnest Rutherfords Gold-Foil-eksperiment?
Her er en sammenbrud af eksperimentet og dets formål:
blomme budding model:
* Denne model, foreslået af J.J. Thomson foreslog, at atomet var en sfære af positivt ladet stof med negativt ladede elektroner indlejret i det, som blommer i en budding.
Rutherfords eksperiment:
* Rutherford dirigerede en stråle af alfa -partikler (positivt ladede partikler) ved et tyndt ark guldfolie.
* Han forventede, at alfa -partiklerne ville passere gennem folien med kun mindre afbøjninger, da blommepudding -modellen forudsagde en diffus fordeling af positiv ladning.
De uventede resultater:
* Meget til hans overraskelse blev en lille procentdel af alfa -partiklerne afbøjet i store vinkler, hvor nogle endda hoppede tilbage mod kilden.
* Dette var et helt uventet resultat, da blommepudding -modellen ikke kunne forklare disse store afbøjninger.
Rutherfords fortolkning:
* Rutherford konkluderede, at den positive ladning i atomet var koncentreret i en meget lille, tæt region i centrum, som han kaldte kernen.
* Han foreslog, at atomet for det meste var tomt rum, med elektroner, der kredsede om kernen.
Virkningen af eksperimentet:
* Rutherfords guldfoleringseksperiment revolutionerede vores forståelse af atomet.
* Den modbevisede blommepudding -modellen og førte til udviklingen af atomets nukleare model, som er grundlaget for moderne atomteori.
I det væsentlige havde Rutherfords eksperiment til formål at teste atomets eksisterende model. Det gjorde det ved at bombardere guldfolie med alfa -partikler og observere deres opførsel. Resultaterne førte til en helt ny forståelse af atomstruktur.
Sidste artikelHvordan påvirker kraft og masse bevægelse?
Næste artikelDen kraft, du udøver på en håndtag, kaldes.?
 Varme artikler
Varme artikler
-
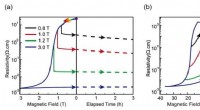 Forskere opdager den fysiske oprindelse af elektroniske faseadskillelsesfænomener i komplekse oxide…Lavtemperatur magnetoresistans efter nul-felt køling. (a) Legeringsfilmens magnetoresistens ved 10 K efter afkøling uden nul. (b) Samme proces som i A, men for den bestilte film på 0,38 K. Kredit:MIAO
Forskere opdager den fysiske oprindelse af elektroniske faseadskillelsesfænomener i komplekse oxide…Lavtemperatur magnetoresistans efter nul-felt køling. (a) Legeringsfilmens magnetoresistens ved 10 K efter afkøling uden nul. (b) Samme proces som i A, men for den bestilte film på 0,38 K. Kredit:MIAO -
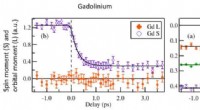 Laserdrevet spin-dynamik i ferrimagneter:Hvordan flyder vinkelmomentet?I starten, Gd besidder ingen vinkelmoment (L =0), og der ses ingen akkumulering under demagnetiseringen, efter at laserpulsen har ramt prøven på tidspunktet nul. I Fe, både S og L falder i samme hasti
Laserdrevet spin-dynamik i ferrimagneter:Hvordan flyder vinkelmomentet?I starten, Gd besidder ingen vinkelmoment (L =0), og der ses ingen akkumulering under demagnetiseringen, efter at laserpulsen har ramt prøven på tidspunktet nul. I Fe, både S og L falder i samme hasti -
 Hybrid enhed høster både mekanisk og magnetisk energiHybrid energihøsteren består af en udkraget bjælke lavet af et magnetostriktivt/piezoelektrisk materiale, der høster både magnetisk og mekanisk energi. Kredit:Xu et al. © 2018 American Institute of Ph
Hybrid enhed høster både mekanisk og magnetisk energiHybrid energihøsteren består af en udkraget bjælke lavet af et magnetostriktivt/piezoelektrisk materiale, der høster både magnetisk og mekanisk energi. Kredit:Xu et al. © 2018 American Institute of Ph -
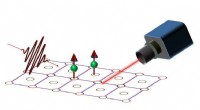 Transformerende magnetisk lagring kan stamme fra visionen om kvanteSkematisk af den foreslåede eksperimentelle opsætning. En intens laserpuls exciterer et ferromagnetisk jernmonolag og genererer højordens harmoniske. De harmoniske signaler opsamles af et kamera; hvis
Transformerende magnetisk lagring kan stamme fra visionen om kvanteSkematisk af den foreslåede eksperimentelle opsætning. En intens laserpuls exciterer et ferromagnetisk jernmonolag og genererer højordens harmoniske. De harmoniske signaler opsamles af et kamera; hvis
- Arkæologer afgraver en gammel faraonisk by i Egypten
- DNA-baseret elektromekanisk switch demonstreret
- Hvad betyder spildt energi?
- Aktiveret grafen laver overlegne superkondensatorer til energilagring
- Hvilke ikke -vedvarende energiressourcer er fossile brændstoffer?
- Hvad er samspillet mellem overfladevand og grundvand i et farvande?


