Hvad er orbitaldiagrammet for Fe?
1. Elektronisk konfiguration:
* Jern har et atomnummer på 26, hvilket betyder, at det har 26 elektroner.
* Den elektroniske konfiguration til jern er: 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3d⁶
2. Orbital diagram:
* 1s: To elektroner fylder 1s orbital (repræsenteret som ↑ ↓).
* 2s: To elektroner fylder 2'erne orbital (↑ ↓).
* 2p: Seks elektroner fylder de tre 2p -orbitaler med en elektron i hver orbital inden parring (↑ ↑ ↑).
* 3s: To elektroner fylder 3'erne orbital (↑ ↓).
* 3p: Seks elektroner fylder de tre 3p orbitaler (↑ ↓ ↑ ↓ ↑ ↓).
* 4S: To elektroner fylder 4S orbital (↑ ↓).
* 3d: Seks elektroner fylder de fem 3D -orbitaler. Efter Hunds regel fylder vi hver orbital med en elektron inden parring:↑ ↑ ↑ ↑ ↑
3. Repræsentation:
Det komplette orbitaldiagram for jern ser sådan ud:
`` `
1S:↑ ↓
2s:↑ ↓
2p:↑ ↑ ↑
3S:↑ ↓
3P:↑ ↓ ↑ ↓ ↑ ↓
4S:↑ ↓
3d:↑ ↑ ↑ ↑ ↑
`` `
Vigtig note: 3D -orbitaler er normalt repræsenteret som et kassediagram med fem kasser, der hver repræsenterer en anden 3D -orbital.
Fortæl mig, hvis du gerne vil have mig til at tegne boksdiagrammet!
Sidste artikelEr en kvart dirigent eller isolator?
Næste artikelEr det muligt, at en partikel har nulhastighed, men stadig har acceleration?
 Varme artikler
Varme artikler
-
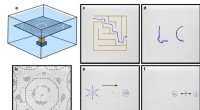 Et overraskende eksperiment åbner vejen til nye partikelmanipulationsmetoder(a-b) Tunge partikler bevæger sig mod antinoder på en neddykket vibrerende plade. (c-d) Enkelte partikler og (e-f) en sværm af partikler bevæger sig på foruddefinerede baner på pladen ved at spille nø
Et overraskende eksperiment åbner vejen til nye partikelmanipulationsmetoder(a-b) Tunge partikler bevæger sig mod antinoder på en neddykket vibrerende plade. (c-d) Enkelte partikler og (e-f) en sværm af partikler bevæger sig på foruddefinerede baner på pladen ved at spille nø -
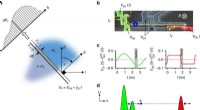 Forskere udvikler tomografiske metoder til at visualisere tilstanden af solitære elektronerElektrontomografiskema ved hjælp af en moduleret barriere. a En ukendt Wigner-fordeling W(E, t) af en periodisk elektronkildeelektron kan filtreres under anvendelse af en lineær-i-tid tærskelenergibar
Forskere udvikler tomografiske metoder til at visualisere tilstanden af solitære elektronerElektrontomografiskema ved hjælp af en moduleret barriere. a En ukendt Wigner-fordeling W(E, t) af en periodisk elektronkildeelektron kan filtreres under anvendelse af en lineær-i-tid tærskelenergibar -
 Internationalt team af fysikere fortsætter søgen efter ny fysikDen kompakte Muon Solenoid-detektor er en detektor til generelle formål på Large Hadron Collider (LHC) i Schweiz, designet til at observere alle nye fysikfænomener, som LHC kan afsløre. Kredit:CERN
Internationalt team af fysikere fortsætter søgen efter ny fysikDen kompakte Muon Solenoid-detektor er en detektor til generelle formål på Large Hadron Collider (LHC) i Schweiz, designet til at observere alle nye fysikfænomener, som LHC kan afsløre. Kredit:CERN -
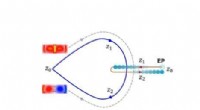 Optisk databehandling drager fordel af ny form for mobilitetModusoverførsel, da de geometriske parametre for bølgelederne omkranser et exceptionelt punkt i bevægelse. Kredit:Wang Bing Tilstandskontrol er afgørende for optisk kommunikation og databehandling
Optisk databehandling drager fordel af ny form for mobilitetModusoverførsel, da de geometriske parametre for bølgelederne omkranser et exceptionelt punkt i bevægelse. Kredit:Wang Bing Tilstandskontrol er afgørende for optisk kommunikation og databehandling
- Sådan beregnes varme absorberet af Solution
- Aktiviteten af alle menneskelige kropssystemer koordineres af hvad?
- Hvad er det rum, der er besat af elektroner, der kaldes?
- Triple-mode transistorer viser potentiale:Forskere introducerer grafenbaserede forstærkere
- Hvordan forhindrer du oxidation af metal?
- Hvorfor er der flere tordenvejr i løbet af sommeren?


