Hvorfor er sagen kontinuerlig i form?
* atomteori: De grundlæggende byggesten af stof er atomer. Atomer er små, udelelige partikler, der kombineres for at danne molekyler og større strukturer. Der er tomt rum mellem disse atomer.
* kvantemekanik: Quantum Mechanics beskriver anfægten af stof på atom- og subatomiske niveauer. Det viser, at der findes stof i diskrete energipakker, kaldet Quanta. Dette betyder, at sagen ikke er uendeligt delbar.
* Bevis: Eksperimenter som spredning af alfa -partikler ved guldfolie (Rutherfords eksperiment) demonstrerede eksistensen af en kerne i atomet, hvilket indebærer et tomt rum i atomet.
Eksempler på, at stof er diskret:
* Vand: Vand er lavet af H2O -molekyler. Der er huller mellem disse molekyler, hvilket gør vand til en væske.
* Metaller: Metaller er lavet af atomer arrangeret i en gitterstruktur. Selvom atomerne er tæt pakket, er der stadig tomt mellemrum mellem dem.
* Gasser: Gasser har meget store mellemrum mellem deres atomer eller molekyler. Dette gør det muligt for dem at komprimeres let.
Imidlertid kan stof vises kontinuerligt ved makroskopiske skalaer. Dette skyldes det store antal involverede atomer. For eksempel ser et stykke træ ud til at være et solidt kontinuerligt materiale, men det består faktisk af et stort antal atomer og molekyler.
Konklusion:
Mens stof kan vises kontinuerligt i store skalaer på et mikroskopisk niveau, består det af diskrete partikler (atomer og molekyler) adskilt af tomt rum. Begrebet "kontinuerligt" stof er en forenkling, der fungerer til mange praktiske formål, men det er ikke en grundlæggende sandhed om stoffet.
 Varme artikler
Varme artikler
-
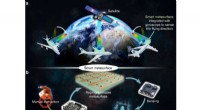 Smarte metamaterialer, der fornemmer og omprogrammerer sig selvSkematisk af en smart metasurface. (a) Illustration af den foreslåede smarte metaoverflade med de selvadaptive omprogrammerbare funktioner uden manuel instruktion. (b) systemet med lukket kredsløb på
Smarte metamaterialer, der fornemmer og omprogrammerer sig selvSkematisk af en smart metasurface. (a) Illustration af den foreslåede smarte metaoverflade med de selvadaptive omprogrammerbare funktioner uden manuel instruktion. (b) systemet med lukket kredsløb på -
 Tekstureret LED giver grønt lys til Li-FiV-gruber på overfladen af en InGaN LED (til venstre) spreder lys ind i enhedens aktive lag, kendt som kvantebrønde (QWer - til højre). Kredit:American Chemical Society. Standard lysdioder (LEDer
Tekstureret LED giver grønt lys til Li-FiV-gruber på overfladen af en InGaN LED (til venstre) spreder lys ind i enhedens aktive lag, kendt som kvantebrønde (QWer - til højre). Kredit:American Chemical Society. Standard lysdioder (LEDer -
 En stjerne er født:Ved hjælp af lasere til at undersøge, hvordan stjernemateriale fremstillesSkudtidsbillede fra et NIF-eksperiment for at studere stjernens nukleosyntese. Solar 3He-3He reaktioner sker i billedets lyse centrum, hvor de meget varme og meget tætte stjernelignende forhold skabes
En stjerne er født:Ved hjælp af lasere til at undersøge, hvordan stjernemateriale fremstillesSkudtidsbillede fra et NIF-eksperiment for at studere stjernens nukleosyntese. Solar 3He-3He reaktioner sker i billedets lyse centrum, hvor de meget varme og meget tætte stjernelignende forhold skabes -
 The Demon in the Machine er kåret som årets fysikbog i StorbritannienPaul Davies nye bog, Dæmonen i maskinen:Hvordan skjulte informationsnet løser livets mysterium, er blevet kåret til årets bog for 2019 af Physics World. Kredit:Arizona State University Paul Davies
The Demon in the Machine er kåret som årets fysikbog i StorbritannienPaul Davies nye bog, Dæmonen i maskinen:Hvordan skjulte informationsnet løser livets mysterium, er blevet kåret til årets bog for 2019 af Physics World. Kredit:Arizona State University Paul Davies


