Forståelse af elektronkapacitet:s vs. p orbitaler forklaret
Her er en oversigt:
* s underniveau:
* Har kun én orbital , som er kugleformet.
* Hver orbital kan maksimalt indeholde to elektroner på grund af Pauli Exclusion Principle (som siger, at ikke to elektroner i et atom kan have det samme sæt af fire kvantetal).
* p underniveau:
* Har tre orbitaler , hver med en håndvægtsform orienteret langs forskellige akser (x, y, z).
* Hver af disse p-orbitaler kan maksimalt indeholde to elektroner , ligesom s orbital.
* Da der er tre p-orbitaler, er det samlede maksimale antal elektroner i et p-underniveau 6 (3 orbitaler x 2 elektroner pr. orbital).
Sammenfattende skyldes forskellen i det maksimale antal elektroner, at p underniveauer har flere orbitaler end s underniveauer.
 Varme artikler
Varme artikler
-
 Snoende hvirvler af elektronerKredit:CC0 Public Domain I Jules Vernes berømte klassiker 20, 000 ligaer under havet , den ikoniske ubåd Nautilus forsvinder ind i Moskenstraumen, et massivt boblebad ud for Norges kyst. I rumme
Snoende hvirvler af elektronerKredit:CC0 Public Domain I Jules Vernes berømte klassiker 20, 000 ligaer under havet , den ikoniske ubåd Nautilus forsvinder ind i Moskenstraumen, et massivt boblebad ud for Norges kyst. I rumme -
 Lysere fremtid for LED'er:NIST introducerer nyt lampekalibreringslaboratoriumEn lyskilde kaldet en FEL-lampe skinner fra et af de nye automatiserede udstyrsborde. Denne tabel indeholder alle de lyskilder, der enten testes eller bruges til at teste en detektor. Kredit:Jennifer
Lysere fremtid for LED'er:NIST introducerer nyt lampekalibreringslaboratoriumEn lyskilde kaldet en FEL-lampe skinner fra et af de nye automatiserede udstyrsborde. Denne tabel indeholder alle de lyskilder, der enten testes eller bruges til at teste en detektor. Kredit:Jennifer -
 En sikker optisk fiber til at levere lys og medicin ind i kroppenEt billede af lyslevering gennem en citratbaseret optisk fiber. Kredit:Dingying Shan / Chenji Zhang / Penn State En fleksibel, biologisk nedbrydelig optisk fiber, der kan levere lys ind i kroppen
En sikker optisk fiber til at levere lys og medicin ind i kroppenEt billede af lyslevering gennem en citratbaseret optisk fiber. Kredit:Dingying Shan / Chenji Zhang / Penn State En fleksibel, biologisk nedbrydelig optisk fiber, der kan levere lys ind i kroppen -
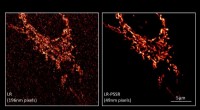 Ny metode kunne demokratisere mikroskopi med forbedret dyb læringEt lavopløsningsbillede af et mitokondrielt netværk (cellens kraftcenter) inde i en kræftcelle (venstre) forbedres ved hjælp af kunstig intelligens (højre). Stillbilledet er taget fra et levende bille
Ny metode kunne demokratisere mikroskopi med forbedret dyb læringEt lavopløsningsbillede af et mitokondrielt netværk (cellens kraftcenter) inde i en kræftcelle (venstre) forbedres ved hjælp af kunstig intelligens (højre). Stillbilledet er taget fra et levende bille
- Alkaline Vs. Basic
- Krateret, der dræbte dinosaurerne, afslører, hvordan knuste sten kan flyde som væske
- Ved at klassificere akvatiske makroinvertebrater baseret på deres bevægelse fortæller det dig om …
- Hvad er et energioverførselsdiagram over et solcellepanel?
- Polymerantistoffer målretter og eliminerer effektivt kræftceller
- Hvordan hjælper luft med at opretholde temperaturen?


