Intermolekylære kræfter:Forståelse af tiltrækningen mellem molekyler
1. Van der Waals styrker:
* Dipol-dipol-interaktioner: Opstår mellem polære molekyler med permanente dipoler. Den positive ende af et molekyle tiltrækker den negative ende af et andet.
* London Dispersion Forces (LDF): Til stede i alle molekyler, også ikke-polære. De opstår fra midlertidige, øjeblikkelige dipoler, der dannes på grund af elektronernes konstante bevægelse. Jo større molekylet er, jo stærkere er LDF.
* Brintbinding: En speciel type dipol-dipol-interaktion, der opstår, når et hydrogenatom er bundet til et meget elektronegativt atom som oxygen, nitrogen eller fluor. Det er den stærkeste type van der Waals-styrke.
2. Ion-dipol-interaktioner:
Opstår mellem en ion (enten positiv eller negativ) og et polært molekyle. Ionen tiltrækkes af den modsat ladede ende af det polære molekyle.
3. Ion-inducerede dipol-interaktioner:
Opstår, når en ion inducerer en midlertidig dipol i et ikke-polært molekyle ved at forvrænge dets elektronsky.
Styrken af intermolekylære kræfter bestemmer mange fysiske egenskaber ved stoffer, såsom:
* Kogepunkt: Stærkere kræfter fører til højere kogepunkter.
* Smeltepunkt: Stærkere kræfter fører til højere smeltepunkter.
* Opløselighed: Lignende intermolekylære kræfter mellem opløst stof og opløsningsmiddel fører til bedre opløselighed.
* Viskositet: Stærkere kræfter fører til højere viskositet (modstand mod strømning).
At forstå typerne og styrkerne af intermolekylære kræfter er afgørende på forskellige områder, herunder kemi, biologi og materialevidenskab.
 Varme artikler
Varme artikler
-
 Ingen flydende helium, men stadig ekstremt sejtSae Woo Nam (til venstre) og Vincent Kotsubo undersøger prototypen til deres nye cryocooler. Kredit:National Institute of Standards and Technology NIST-forskere har udtænkt et nyt hybridsystem til
Ingen flydende helium, men stadig ekstremt sejtSae Woo Nam (til venstre) og Vincent Kotsubo undersøger prototypen til deres nye cryocooler. Kredit:National Institute of Standards and Technology NIST-forskere har udtænkt et nyt hybridsystem til -
 Konform meta -overfladebelægning eliminerer krydstale og krymper bølgeledereStavformet bølgeleder med to kvasi-todimensionale konforme belægninger, der afskærer bølgelederen fra krydstale og blokerer og tillader bølgelederen at være mindre. Kredit:Werner Lab / Penn State
Konform meta -overfladebelægning eliminerer krydstale og krymper bølgeledereStavformet bølgeleder med to kvasi-todimensionale konforme belægninger, der afskærer bølgelederen fra krydstale og blokerer og tillader bølgelederen at være mindre. Kredit:Werner Lab / Penn State -
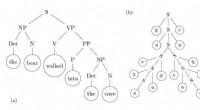 Fysiker anvender statistiske mekanikteorier til at forklare, hvordan børn lærer et sprogIllustrative afledningstræer for (a) simpel engelsk sætning, og (b) RNA sekundær struktur (efter [6]). Sidstnævnte er en afledning af sekvensen gacuaagcugaguc og viser dens foldede struktur. Terminals
Fysiker anvender statistiske mekanikteorier til at forklare, hvordan børn lærer et sprogIllustrative afledningstræer for (a) simpel engelsk sætning, og (b) RNA sekundær struktur (efter [6]). Sidstnævnte er en afledning af sekvensen gacuaagcugaguc og viser dens foldede struktur. Terminals -
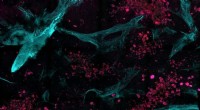 Ikke-invasiv billeddannelsesmetode ser kræft på molekylært niveauForskerne kombinerede multiphotonmikroskopi med automatiseret billed- og statistisk analyse algoritmer for at skelne mellem sundt og sygt væv. I dette billede, samlet i en helt etiketfri, ikke -invasi
Ikke-invasiv billeddannelsesmetode ser kræft på molekylært niveauForskerne kombinerede multiphotonmikroskopi med automatiseret billed- og statistisk analyse algoritmer for at skelne mellem sundt og sygt væv. I dette billede, samlet i en helt etiketfri, ikke -invasi
- Hvilken isotop bruges til at studere skjoldbruskkirtlen?
- Hvor kommer hæmatitrock fra?
- Den peptidoglycan af bakteriecellevæggen indeholder en kulhydratmatrix, der er knyttet sammen, vær…
- Undersøgelse afslører dagligdags teknologi hjælper med at bekæmpe ensomhed
- Hvad betyder encellulær organisme?
- Hvordan bakterier reagerer så hurtigt på ydre ændringer


