Intermolekylære kræfter i væske F2:Forståelse af Londons spredningskræfter
Her er hvorfor:
* F₂ er et ikke-polært molekyle: Fluoratomer har samme elektronegativitet, så F-F-bindingen er upolær. Hele F₂-molekylet mangler et permanent dipolmoment.
* London spredningskræfter er til stede i alle molekyler: Disse kræfter opstår fra midlertidige, øjeblikkelige fluktuationer i elektronfordelingen, hvilket skaber midlertidige dipoler, der inducerer dipoler i nabomolekyler. Selvom F₂ er upolær, forekommer disse midlertidige fluktuationer stadig.
* Andre kræfter er fraværende: F₂ har ikke hydrogenbinding (ingen hydrogenatomer direkte bundet til stærkt elektronegative atomer) eller dipol-dipol-interaktioner (på grund af dens upolære natur).
Derfor er London-spredningskræfter den eneste signifikante intermolekylære kraft, der er til stede i flydende F2.
 Varme artikler
Varme artikler
-
 Under pres, squishy forbindelse reagerer på bemærkelsesværdige måderDa en forbindelse af mangansulfid komprimeres i en diamantamboltcelle, den gennemgår dramatiske overgange. I denne illustration, interaktionen mellem mangan (Mn) atomære ioner (lilla cirkler) og disul
Under pres, squishy forbindelse reagerer på bemærkelsesværdige måderDa en forbindelse af mangansulfid komprimeres i en diamantamboltcelle, den gennemgår dramatiske overgange. I denne illustration, interaktionen mellem mangan (Mn) atomære ioner (lilla cirkler) og disul -
 Myggeøje inspirerer til en kunstig sammensat linseForskere har udviklet sammensatte linser inspireret af myggeøjet. Kredit:American Chemical Society Enhver, der har prøvet at slå en irriterende myg, ved, hvor hurtigt insekterne kan undslippe en h
Myggeøje inspirerer til en kunstig sammensat linseForskere har udviklet sammensatte linser inspireret af myggeøjet. Kredit:American Chemical Society Enhver, der har prøvet at slå en irriterende myg, ved, hvor hurtigt insekterne kan undslippe en h -
 Fysikere udvikler et effektivt modem til et fremtidigt kvanteinternetGarching kvantemodem:Krystalskiven med kvantebits af erbium atomer (pile) er i midten, det frem og tilbage reflekterede infrarøde lys er angivet af de røde skiver. Kredit:Christoph Hohmann (MCQST)
Fysikere udvikler et effektivt modem til et fremtidigt kvanteinternetGarching kvantemodem:Krystalskiven med kvantebits af erbium atomer (pile) er i midten, det frem og tilbage reflekterede infrarøde lys er angivet af de røde skiver. Kredit:Christoph Hohmann (MCQST) -
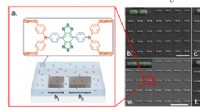 Engineering enkelt-molekyle fluorescens med asymmetriske nano-antenner(a) Skematisk af dobbelt-bar nano-antenne belagt med AIEE1000 molekyler (sorte dobbelte ende pile) i PMMA (lyseblå) på glas substrat (lyse grå). Indsat viser den kemiske struktur af AIEE1000. (b-g) SE
Engineering enkelt-molekyle fluorescens med asymmetriske nano-antenner(a) Skematisk af dobbelt-bar nano-antenne belagt med AIEE1000 molekyler (sorte dobbelte ende pile) i PMMA (lyseblå) på glas substrat (lyse grå). Indsat viser den kemiske struktur af AIEE1000. (b-g) SE
- Tarmbakterie forårsager indirekte symptomer ved at ændre frugtflues mikrobiom
- Hvordan redegør du for det rigelige kvarts og mangelfeldspat i de fleste jord?
- Fjerndetektion af vira på overflader
- Bivirkningerne af kvantefejlkorrektion og hvordan man håndterer dem
- Forskere bruger standard kontorscanner som et værktøj til jordfarveevaluering
- Skiftende strømme rejser kun i en retning og er den type strøm, som de fleste elektroniske enheder…


