I hvilken tilstand er de fleste elementer i?
Her er hvorfor:
* Stærke attraktioner: Atomer i faste stoffer holdes sammen af stærke kræfter, som metallisk binding, ionisk binding eller kovalent binding. Disse kræfter holder atomerne tæt pakket og i et fast arrangement.
* Lav temperatur: Rumtemperatur er relativt lav sammenlignet med de energier, der kræves for at bryde bindingerne mellem atomer i faste stoffer.
* Undtagelser: Der er nogle få undtagelser, som:
* Gasser: Elementer som brint, helium, nitrogen, ilt, fluor, klor, neon, argon, krypton, xenon og radon er gasser ved stuetemperatur. Deres atomer har svage attraktioner.
* væsker: Kviksølv og brom er de eneste to elementer, der er væsker ved stuetemperatur. De har svagere bindinger end faste stoffer, men stærkere bindinger end gasser.
Så selvom der er nogle undtagelser, findes langt de fleste elementer som faste stoffer ved stuetemperatur.
 Varme artikler
Varme artikler
-
 Top 5 måder, hvor brande starterEt hus brænder under Woolsey -branden den 9. november, 2018, i Malibu, Californien. Beboere i Thousand Oaks er truet af antændelsen af to nærliggende farlige naturbrande, herunder Woolsey Fire, som
Top 5 måder, hvor brande starterEt hus brænder under Woolsey -branden den 9. november, 2018, i Malibu, Californien. Beboere i Thousand Oaks er truet af antændelsen af to nærliggende farlige naturbrande, herunder Woolsey Fire, som -
 Hvad er forskellen mellem et Tornado -ur og en advarsel?En tornado rører ved nær Dodge City, Kansas, 24. maj kl. 2016. Ryan McGinnis/Getty ImagesHvad der skete, var netop dette:Vinden begyndte at skifte, huset til at slå op og pludselig begyndte hængslerne
Hvad er forskellen mellem et Tornado -ur og en advarsel?En tornado rører ved nær Dodge City, Kansas, 24. maj kl. 2016. Ryan McGinnis/Getty ImagesHvad der skete, var netop dette:Vinden begyndte at skifte, huset til at slå op og pludselig begyndte hængslerne -
 Hvis regnbuer er cirkulære,Hvorfor ser vi kun buer? De fleste regnbuer, vi ser, ligner buer, fordi de delvist er blokeret af jorden og horisonten. I virkeligheden, alle regnbuer er komplette cirkler, som denne fotografe
Hvis regnbuer er cirkulære,Hvorfor ser vi kun buer? De fleste regnbuer, vi ser, ligner buer, fordi de delvist er blokeret af jorden og horisonten. I virkeligheden, alle regnbuer er komplette cirkler, som denne fotografe -
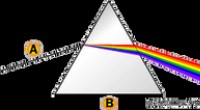 Hvad forårsager en regnbue?For to dage siden, dagens spørgsmål var Hvorfor er himlen blå? Af en eller anden grund, der udløste en oversvømmelse af Hvad forårsager en regnbue? spørgsmål, så lad os gå gennem regnbuernes natur.
Hvad forårsager en regnbue?For to dage siden, dagens spørgsmål var Hvorfor er himlen blå? Af en eller anden grund, der udløste en oversvømmelse af Hvad forårsager en regnbue? spørgsmål, så lad os gå gennem regnbuernes natur.
- Sådan laver du et hårdt kogt æg Gå ind i en koksflaske
- Et enkelt molekyle i sigte:Intelligente molekyler
- Måler tid uden ur
- Hvad er de generelle matematiske operationer, du bruger, når du konverterer en SI -enhed til en and…
- Kemi Nobel for at bruge evolution til at skabe nye proteiner
- Mexico erkender, at banker blev hacket; tab ukendt


