Bygge broer med vandmolekyler
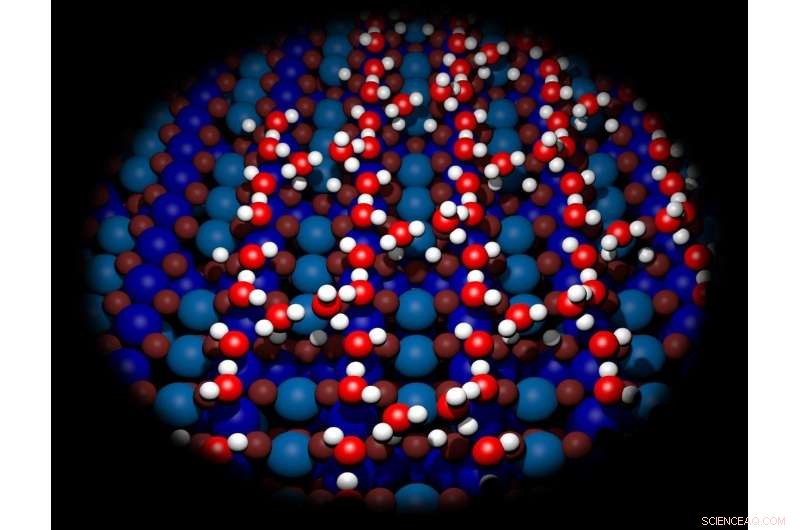
Vandmolekyler danner komplekse strukturer på en jernoxidoverflade. Kredit:Vienna University of Technology
Et hold ved TU Wien har nu beviset bag spekulationerne om, at vandmolekyler kan danne komplekse brolignende strukturer, når de akkumuleres på mineralske overflader.
Vand er en ekstremt kompleks væske. Den måde, hvorpå separate vandmolekyler akkumuleres på forskellige materialer, har en afgørende indflydelse på rigtig mange processer, herunder korrosion og forvitring, og er nøglen til at sikre, at katalysatorer fungerer optimalt. Et hold baseret på TU Wien har nu formået at afsløre mysteriet bag strukturen af vandmolekyler på jernoxidoverflader, og deres arbejde har afsløret, at vandmolekyler kan danne komplekse strukturer, der minder om broer, som spiller en væsentlig rolle, når det kommer til kemiske reaktioner på overfladen.
Vandets særlige egenskaber
"Det, der gør vandmolekyler unikke, er, at de kan danne brintbrobindinger, " forklarer prof. Gareth Parkinson fra Institute of Applied Physics ved TU Wien. "Den elektriske ladningsfordeling er ikke ens. Oxygenatomet er svagt negativt ladet, mens brintatomerne er let positivt ladede." Som et resultat, bindinger kan dannes mellem vandmolekyler – de berømte brintbrobindinger – eller endda mellem et vandmolekyle og andre typer molekyler.
Eftervirkningerne af dette er vidtrækkende. For eksempel, brintbrobindinger er årsagen til, at vand skal nå den høje temperatur på 100°C, før det koger. De er også en nøglefaktor i strukturen af proteiner.
Disse bindinger kommer endda i spil gang på gang for fuldstændig uvidenskabelige påstande, som folk hævder, tillader de, at mystisk 'information' kan opbevares i vand. Dette er fysisk umuligt, fordi brintbrobindinger slet ikke er særlig stærke og nedbrydes igen på et splitsekund i flydende vand. Alligevel, du kan se meget forskellige resultater, når vandmolekyler samler sig på overflader, hvor det er utroligt komplekst, stabile strukturer dannes ved lave temperaturer.
Mulighedernes rige
"Der havde allerede været indirekte indikationer på, at denne type struktur dannedes, " siger Ulrike Diebold (TU Wien). "Men for virkelig at gøre vandets struktur synlig på jernoxidoverflader, vi var nødt til at optimere de allerbedste state-of-the-art måleteknikker yderligere og virkelig rykke grænserne for, hvad der er muligt."
Til at begynde med, en stråle af vandmolekyler blæses på overfladen i et vakuum ved lav temperatur. Overfladen varmes derefter forsigtigt op til en temperatur på omkring -30°C, bevirker, at vandstrukturerne gradvist brydes op. Vandmolekylerne løsner sig fra overfladen en efter en og opsamles af en detektor. "Vi kan måle præcis, hvor mange vandmolekyler der forlader overfladen ved en bestemt temperatur. Vi kan så tage denne information til at beregne bindingsenergien, hvilket igen giver os mulighed for at identificere den type molekylestrukturer vi har at gøre med, " forklarede Gareth Parkinson.
På samme tid, en speciel vibrationssikker, højtydende mikroskop blev brugt til at producere billeder i høj opløsning af overfladen, så vandstrukturerne rent faktisk kunne ses. Ud over dette, sofistikerede computersimuleringer blev udviklet som en måde at forklare den geometriske placering af vandmolekylerne på kvanteniveau. "Endelig har vi tre værktøjer til rådighed, som giver os mulighed for at studere vandstrukturerne, og det er det, der skal til, hvis du vil have pålidelige resultater, " siger Gareth Parkinson. "Alle tre analyser matcher perfekt, Det efterlader os med stor tillid til at konkludere, at vi nu forstår dannelsen af vandstrukturer på jernoxidoverflader."
Beviserne viser, at der dannes flere strukturer:det er sjældent, at et enkelt vandmolekyle sidder alene på overfladen, med vandmolekyler i stedet for at samle sig i par eller grupper af tre. Så har du mere komplekse strukturer bestående af seks eller otte molekyler, som spænder over jernoxidets overflade som elliptisk buede broer.
"Vores primære mål var at udvikle de analytiske metoder til det punkt, at vi kunne opnå uigendrivelige beviser for disse molekylære strukturer. Og det var, hvad vi gjorde, ", siger Ulrike Diebold. "Den metode, vi brugte her til jernoxid, kan også anvendes på andre materialer."
 Varme artikler
Varme artikler
-
 Sølv forbedrer effektiviteten af solceller i monokornlagNæste generations letvægts, fleksible monograin-lagsolcelle udviklet af TalTech-forskere. Kredit:Professor Jüri Krustok Som et resultat af deres toårige fælles projekt, materialeforskerne fra Tall
Sølv forbedrer effektiviteten af solceller i monokornlagNæste generations letvægts, fleksible monograin-lagsolcelle udviklet af TalTech-forskere. Kredit:Professor Jüri Krustok Som et resultat af deres toårige fælles projekt, materialeforskerne fra Tall -
 Ædelmetalklynger kan forbedre ydeevnen af katalysatorer og spare ressourcerSkematisk fremstilling af en ædelmetalkatalysator med inaktive enkelte atomer (venstre) og aktive klynger (højre; ædelmetal:hvid; bæremetal:gul; oxygen:rød). Kredit:Florian Maurer, SÆT Milliarder
Ædelmetalklynger kan forbedre ydeevnen af katalysatorer og spare ressourcerSkematisk fremstilling af en ædelmetalkatalysator med inaktive enkelte atomer (venstre) og aktive klynger (højre; ædelmetal:hvid; bæremetal:gul; oxygen:rød). Kredit:Florian Maurer, SÆT Milliarder -
 Enzymbiofabrikker til forbedring af navlestrengsblodtransplantationerForskerne viste, at deres gær- og silkeorm-afledte enzym langt bedre end kommercielle kilder til enzymet fremstillet i standard ekspressionssystemer. Kredit:KAUST; Heno Hwang En ny måde at produce
Enzymbiofabrikker til forbedring af navlestrengsblodtransplantationerForskerne viste, at deres gær- og silkeorm-afledte enzym langt bedre end kommercielle kilder til enzymet fremstillet i standard ekspressionssystemer. Kredit:KAUST; Heno Hwang En ny måde at produce -
 Ny genetisk metode forbedrer enzymets effektivitetGregg Beckham (til venstre), Christopher Johnson, og Jeffery Linger er medforfattere af en ny forskerartikel, der beskriver, hvordan de forbedrede effektiviteten af et enzym ved nedbrydning af bioma
Ny genetisk metode forbedrer enzymets effektivitetGregg Beckham (til venstre), Christopher Johnson, og Jeffery Linger er medforfattere af en ny forskerartikel, der beskriver, hvordan de forbedrede effektiviteten af et enzym ved nedbrydning af bioma
- Karakteristika for påtrengende klipper
- Ny sensorteknologi muliggør superfølsom live overvågning af menneskelige biomolekyler
- Virkningerne af nuklear stråling på miljøet
- Karakteristika ved snegle & snegle
- Hvordan man laver en model af en Avalanche
- Digitalisering har vist sig at være et vigtigt klimaværktøj


