Smartere lægemiddelfrigivelse takket være kontrol over indkapsling
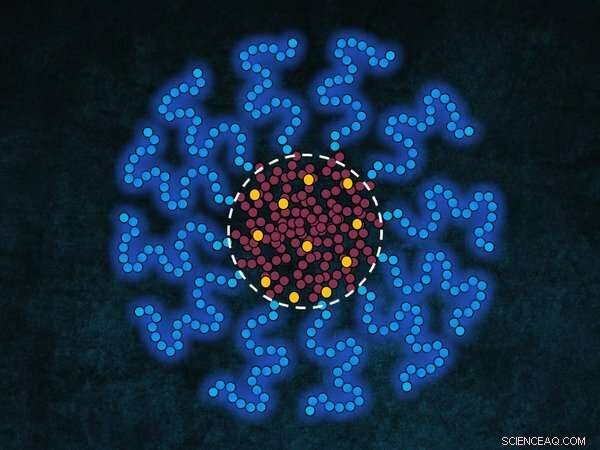
Skematisk figur af en micelle - bestående af en hydrofil skal (blå haler) og en hydrofob kerne (røde haler) - indkapslende lægemiddelmolekyler (gul). Lægemiddelmolekylerne samles for det meste ved kerne-skal-grænsefladen (stiplet-hvid linje) af micellen, hvis koncentrationen af lægemidlet er under opløsningsmidlets vandopløselighed, mens hvis koncentrationen er over opløseligheden, samler de sig i kernen. Kredit:Alessandro Ianori
Forskere ved Eindhoven University of Technology og Utrecht University har opdaget de parametre, der styrer indkapslingen af lægemidler. Dette giver mere kontrol over langsom og stabil frigivelse af lægemidler hos patienter. I øvrigt, at designe indkapslinger til nye lægemidler vil nu kræve langt færre eksperimenter, hvilket giver hurtigere og billigere udvikling af lægemidler. Forskerne mener, at dette arbejde vil have en betydelig indvirkning på det biomedicinske område og design af fremtidige lægemidler.
Mange lægemidler er hydrofobe - de opløses ikke godt i vand - hvilket gør lægemiddellevering hos patienter problematisk. En mulig løsning er at indkapsle lægemidlerne i små pakninger, der er hydrofobe (vandafvisende) på indersiden og hydrofile (vandopløselige) på ydersiden. Lægemidlerne vil akkumulere i indersiden af disse pakker, og transporten af lægemidlet i hele patientens krop bliver meget lettere. Pakkerne består ofte af tilhørende overfladeaktive stoffer, som er farmaceutisk godkendte. Når det er opløst i vand, en fysiologisk løsning, eller blod, disse molekyler orienterer deres hydrofobe del mod den indre kerne (med affinitet for de uopløselige lægemidler) og deres hydrofile side mod ydersiden, danner en sfærisk 'pakke', kaldet en micelle.
Opholdsstedet i en micelle
Transport af stoffer i hele kroppen på denne måde har været mulig i årtier, men først nu forstår forskere, hvilke faktorer der præcist dikterer, hvor stofferne inde i micellen samles. Denne rumlige fordeling kan dramatisk påvirke frigivelseshastigheden af lægemidlerne inde i en patient. Nogle lægemidler koncentrerer sig i midten af den hydrofobe kerne af micellen og frigives langsomt, hvilket er ønskeligt for lægemiddeloptagelsen af en patient. Andre lægemidler samles ved kerne-shell-grænsefladen på micellen og frigives typisk hurtigt. Derfor, styring af placeringen af lægemidlerne i micelleindkapslingen styrer frigivelseshastigheden af lægemidlerne.
Brug af et farvestof til at spore medicin
For at undersøge, hvor uopløselige stoffer samles, forskerne brugte Nile Red, et farvestofmolekyle, der ligner størrelsen og opløseligheden af typiske lægemidler. Farvestoffet har en meget smart egenskab:det absorberer ikke kun en bestemt lysfarve, men også at farven afhænger af dens miljø. Hvis farvestoffet er opløst i rent vand, det absorberer lys af en anden farve, end hvis der også er noget alkohol opløst i vandet. Ændring af vand/alkohol -forholdet er en smart måde at simulere et godt opløsningsmiddel eller et dårligt opløsningsmiddel til farvestoffet. Dette er analogt med at arbejde med et vandopløseligt lægemiddel eller et uopløseligt lægemiddel. Ved at måle lysabsorberingen, forskerne kunne bestemme, hvor meget farvestof der blev samlet i kernen af micellen, og hvor meget ved kernen-shell-grænsefladen.
Eksperimenter kombineret med computersimuleringer
For at bekræfte deres fund, forskerne lavede computersimuleringer for at bestemme placeringen af de opløste lægemidler og formen på blokcopolymeren micelle. Beregningerne afslører arrangementet af komponenterne inden for og uden for micellen, gør det muligt at vurdere de foretrukne områder af lægemidlet.
Af eksperimenterne og beregningerne blev det konkluderet, at det foretrukne område af lægemidlet inde i blokcopolymermicellerne for det meste bestemmes af koncentrationen og opløseligheden af lægemiddelmolekylerne i det omgivende medium (vand/fysiologisk medium/blod). Hvis koncentrationen af lægemidlet er under opløsningsmidlets vandopløselighed, samler lægemiddelmolekylerne sig ved micelle-shell-grænsefladen, mens hvis koncentrationen er over opløseligheden, samler de sig i kernen.
Færre forsøg med fejl
Dagens lægemiddelindkapslingsforskning domineres af forsøg med fejl. Resultaterne rapporteret i denne undersøgelse muliggør lettere og billigere udvikling af smarte lægemidler. Dette vil bidrage til at reducere bivirkninger forbundet med terapi og lette oprettelsen af personlige terapeutiske behandlinger, hvor frigivelsen af lægemidlet tilpasses patientens individuelle behov.
 Varme artikler
Varme artikler
-
 Rettelse til synkrotronforskningsfejl kan forbedre resultaterneKurt Nienaber (tv) og Graham George. Kredit:University of Saskatchewan Forskere fra University of Saskatchewan har fundet ud af, at kemikalier, der normalt bruges til at beskytte prøver i synkrotr
Rettelse til synkrotronforskningsfejl kan forbedre resultaterneKurt Nienaber (tv) og Graham George. Kredit:University of Saskatchewan Forskere fra University of Saskatchewan har fundet ud af, at kemikalier, der normalt bruges til at beskytte prøver i synkrotr -
 Solar fordamper tilbyder en frisk rute til ferskvandEn selvrensende anordning lavet af træ har til formål at gøre småskala afsaltning mere praktisk. Kredit:John T. Consoli/University of Maryland Omkring en milliard mennesker verden over mangler adg
Solar fordamper tilbyder en frisk rute til ferskvandEn selvrensende anordning lavet af træ har til formål at gøre småskala afsaltning mere praktisk. Kredit:John T. Consoli/University of Maryland Omkring en milliard mennesker verden over mangler adg -
 Hvad bestemmer mængden af kemisk energi, et stof har?Bindingerne, der holder molekyler sammen, indeholder den kemiske energi, der er tilgængelig i et stof. Imidlertid er en kemisk reaktion en kompleks dans af atomer og molekyler. Forskellige reaktion
Hvad bestemmer mængden af kemisk energi, et stof har?Bindingerne, der holder molekyler sammen, indeholder den kemiske energi, der er tilgængelig i et stof. Imidlertid er en kemisk reaktion en kompleks dans af atomer og molekyler. Forskellige reaktion -
 Åndeanalysator i skoæskestørrelse opdager dødelig lungesygdom hurtigere, mere præcist end læge…Ser man ind i det beskyttende betræk af en bærbar åndedrætsmonitor udviklet af University of Michigan, der hurtigt og præcist kan detektere akut respiratorisk distress syndrome (ARDS) i den kritiske a
Åndeanalysator i skoæskestørrelse opdager dødelig lungesygdom hurtigere, mere præcist end læge…Ser man ind i det beskyttende betræk af en bærbar åndedrætsmonitor udviklet af University of Michigan, der hurtigt og præcist kan detektere akut respiratorisk distress syndrome (ARDS) i den kritiske a
- Ultralow-power hukommelse bruger størrelsesordener mindre strøm end andre enheder
- Atmosfæriske forskere identificerer den reneste luft på jorden i den første undersøgelse af sin …
- Ghosns tilbageholdelse forlænget til 11. januar
- Hvordan reagerer Pacific Walker-cirkulationen på stærk tropisk vulkanisme?
- Italienske kunstbetjente uden vagt finder plyndret statue i belgisk butik
- Forskere sprænger jern med kraftige røntgenstråler, så se dens elektroner omarrangere


