Molekylære beholdere til sekvestrering af neurotransmitterlægemidler i vand
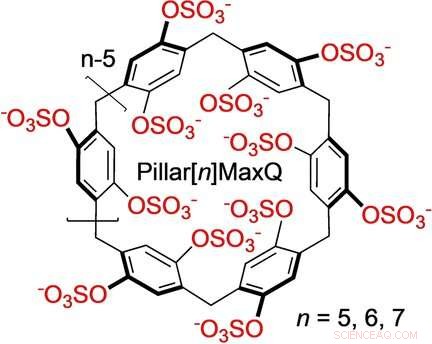
"Pillar[n]MaxQ:En ny værtsfamilie med høj affinitet til sekvestration i vand." Kredit:Angewandte Chemie International Edition
Molekylære beholdere, der fjerner stoffer, toksiner, eller ildelugtende stoffer fra miljøet kaldes sekvestreringsmidler. Forskere har udviklet en klasse af molekylære beholdere, der specifikt sekvestrerer neurotransmitterantagonister. De tøndeformede molekyler kaldet Pillar[n]MaxQ binder neuromuskulært blokerende kemikalier 100, 000 gange mere stramt end etablerede makrocykliske afgiftningsmidler, rapporterer forskerne i tidsskriftet Angewandte Chemie .
Molekylære beholdere af cyclodextrin-typen sekvestrerer deres mål ved kompleksdannelse. De ring- eller tøndeformede molekyler genkender målmolekylernes molekylære træk og trækker dem ind i det centrale hulrum ved hjælp af hydrofobe kræfter. Når først målmolekylet er inde i denne molekylære beholder, den er neutraliseret. Denne vært-gæst kompleksering er den mekanisme, hvorved cyclodextriner, som er store, ringformede sukkermolekyler, fjerne ubehagelige lugte.
Imidlertid, cyclodextriner er ikke særlig specifikke og fejler for de fleste alkaloider - en klasse af nitrogenholdige kemikalier, herunder neurotransmittere og mange ulovlige stoffer. For disse forbindelser, en klasse af molekylære beholdere kaldet pillararener ser ud til at være nyttige. De holder alkaloiderne tæt bundet i deres pillararen-hulrum ved at vikle en ringvæg af aromatiske benzenenheder omkring det kulbrinterige molekylelegeme.
Lyle Isaacs og hans forskerhold fra University of Maryland har videreudviklet strukturen af pillararenerne for at gøre vært-gæst-interaktionerne stærkere og mere specifikke. "Vi forestillede os at skabe en højere negativ ladningstæthed omkring mundingen af hulrummet ved at introducere sure sulfatfunktionelle grupper, " skrev forfatterne. De negativt ladede sulfatgrupper tiltrækker og binder kvaternære ammoniumioner, som er et kendetegn for flere klinisk vigtige neuromuskulære blokerende midler. Sulfatgrupperne stivnede også tøndernes molekylære struktur, fandt forskerne, så lægemiddelgæsten jævnt blev trukket ind i hulrummet af hydrofobe kræfter.
Forskerne døbte de molekylære beholdere Pillar[n]MaxQ, hvor n angiver en målstørrelsesafhængig diameter, der er variabel. De observerede, at denne klasse af sekvestreringsmidler binder de neuromuskulære blokkere op til 100, 000 gange tættere end cyclodextrinbeholderen Sugammadex, som er i klinisk brug. I øvrigt, sekvestreringsmidlet diskriminerede acetylcholin, et naturligt transmitterstof af nerveimpulser i det centrale og perifere nervesystem, som ikke bør sekvestreres.
Forfatterne målte vært-gæst kompleksdannelsesaktiviteterne af Pillar[n]MaxQ ved titreringsundersøgelser, der involverede kalorimetri og kernemagnetisk resonans af gæstemolekylerne. Da pillararener også har vist sig at vende virkningen af neuromuskulære midler hos rotter, forskerne sigter mod at studere de nye Pillar[n]MaxQ-sekvestreringshandlinger i dyremodeller. På grund af den høje binding og specificiteten af de kemisk skræddersyede molekylære beholdere, de er sikre på, at de vil observere positive resultater.
 Varme artikler
Varme artikler
-
 Borat bioaktivt glas i nanoskala:Et næste generations materiale til hudhelingBorat bioaktivt glas i nanoskala. Kredit:MA Kun For nylig, ved hjælp af en steady-state stærk magnetfelt eksperimentel enhed, forskere konstruerede bioaktivt boratglas i nanoskala (Nano-HCA@BG), s
Borat bioaktivt glas i nanoskala:Et næste generations materiale til hudhelingBorat bioaktivt glas i nanoskala. Kredit:MA Kun For nylig, ved hjælp af en steady-state stærk magnetfelt eksperimentel enhed, forskere konstruerede bioaktivt boratglas i nanoskala (Nano-HCA@BG), s -
 Forskere identificerer enzym, der er ansvarligt for at hjælpe kræfttumorer med at sprede sigSteven Van Doren afslørede, hvordan et kræftkritisk enzym er placeret på celleoverflader. Kredit:University of Missouri-Columbia Forskere ved University of Missouri har opdaget, hvordan et kræftkr
Forskere identificerer enzym, der er ansvarligt for at hjælpe kræfttumorer med at sprede sigSteven Van Doren afslørede, hvordan et kræftkritisk enzym er placeret på celleoverflader. Kredit:University of Missouri-Columbia Forskere ved University of Missouri har opdaget, hvordan et kræftkr -
 Mekanistisk grundlag for iltfølsomhed i titaniumMekanisk adfærd af ren Ti, Ti-0,1O, og Ti-0,3O legeringer ved stuetemperatur (RT) (~300 K) og kryogen temperatur (~100 K). (A) Repræsentative tekniske spændings-tøjningskurver for de tre legeringer me
Mekanistisk grundlag for iltfølsomhed i titaniumMekanisk adfærd af ren Ti, Ti-0,1O, og Ti-0,3O legeringer ved stuetemperatur (RT) (~300 K) og kryogen temperatur (~100 K). (A) Repræsentative tekniske spændings-tøjningskurver for de tre legeringer me -
 Studiet producerer de klareste billeder til dato af HSV-1, virus, der forårsager forkølelsessårForskere brugte en metode kaldet subparticle raffinement til at fange detaljerede strukturelle oplysninger om HSV-1 partiklen. Kredit:California NanoSystems Institute ved UCLA UCLA-forskere har pr
Studiet producerer de klareste billeder til dato af HSV-1, virus, der forårsager forkølelsessårForskere brugte en metode kaldet subparticle raffinement til at fange detaljerede strukturelle oplysninger om HSV-1 partiklen. Kredit:California NanoSystems Institute ved UCLA UCLA-forskere har pr
- Forskere finder omkostningseffektive løsninger på sedimentafstrømning og anden landbaseret forure…
- Forskere identificerer sammenhængen mellem planternes nitrogenoptagelse og reduktion af drivhusgase…
- Forskere 3-D print metamaterialer med nye optiske egenskaber
- Menneskeheden på Mars? Teknisk muligt, men ingen rejse i horisonten
- Hvordan man beregner mol af produkter Produced
- Forskere udnytter vira til at spalte vand:Et afgørende skridt i retning af at omdanne vand til brin…


