Hvad er variabel valens?
Elektroner eksisterer i kredsløb omkring en atomkern. Jo højere kredsløbsnummeret er, desto større er afstanden mellem elektronerne fra kernen. Atomer forsøger at opnå en stabil tilstand, der ligner den for de ædle gasser eller de inerte elementer i deres yderste kredsløb ved at acceptere eller donere elektroner. Denne egenskab kaldes atomets valens.
TL; DR (for længe, ikke læst)
Nogle elementer adskiller sig i deres evne til at kombinere med andre elementer afhængigt af reaktionens art ; denne egenskab hedder variabel valens. For eksempel udviser jern i jernoxid en valens på +2, mens det i ferrioxid har en valens på +3.
Valens og binding
Elektronerne i kredsløb tættest på kernen holdes tættere i forhold til dem i de ydre kredsløb. Atomer stræber efter at opnå den elektroniske tilstand, der ligner den af den inerte gas, som den er tættest i det periodiske bord. De gør dette ved at donere overskydende elektroner til et andet atom eller ved at acceptere elektroner fra et andet atom. Når disse valenselektroner doneres eller accepteres, er der dannelse af en ionbinding mellem de deltagende atomer. Når atomer deler valenselektronerne mellem hinanden, resulterer det i dannelse af en kovalent binding.
Variabel Valens
Visse elementer kombinerer med andre atomer, donerer, accepterer eller deler elektroner i forskellige proportioner afhængigt af reaktionens art. For eksempel kombinerer jern med ilt for at danne ferrooxid såvel som ferric oxide. Ved dannelsen af jernholdigt oxid udviser jern en valens på +2, mens den i ferric oxide har en valens på +3. Dette kaldes variabel valens.
Elementer med variabel valency
Overgangsmetaller nikkel, kobber, tin og jern udviser variabel valens. Nonmetals som nitrogen og oxygen viser også variabel valens. Produkterne dannet som et resultat af reaktion med de forskellige valentatomer adskiller sig i deres egenskaber. For eksempel er ferrooxid i det ovenstående eksempel ikkemagnetisk, mens jernoxid har magnetisk karakter. Tilsvarende viser hydrogen en valens af +2 i hydrogenperoxid og en valens på +1 i tilfælde af vand; hydrogenperoxid er stærkt surt i naturen, mens vand er neutralt.
Variabelt valens repræsentation
Det er en praksis at angive valensen af et element med variabel valens ved at bruge det korrekte romertal som et superskript placeret ved siden af elementets symbol. Eksempelvis viser skrivning af PVCl5, at fosfor har en valens på +5 i phosphorpentachlorid.
Sidste artikelHvad repræsenterer periodens nummer?
Næste artikelForskellen mellem isotoper af det samme element
 Varme artikler
Varme artikler
-
 Hvorfor er kobbersulfatblåt?Som mange overgangsmetalkomplekser er kobber (II) sulfatpentahydrat farvet; krystaller af dette smukke stof er en lys nuance af blå. Dens farve stammer fra kemi og fysik i dets sammensætning - elle
Hvorfor er kobbersulfatblåt?Som mange overgangsmetalkomplekser er kobber (II) sulfatpentahydrat farvet; krystaller af dette smukke stof er en lys nuance af blå. Dens farve stammer fra kemi og fysik i dets sammensætning - elle -
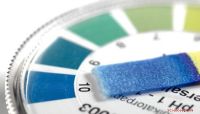 Sådan bruges lakmuspapirerNår du vil bestemme surhedsgraden eller alkaliteten af en flydende eller vandopløselig gas, er den nemmeste måde at udføre en lakmustest. Testen kræver lakmuspapir, som er smalle strimler af papir b
Sådan bruges lakmuspapirerNår du vil bestemme surhedsgraden eller alkaliteten af en flydende eller vandopløselig gas, er den nemmeste måde at udføre en lakmustest. Testen kræver lakmuspapir, som er smalle strimler af papir b -
 Sådan bestemmes pH ud fra pKaStyrken af en syre måles ved både dens pH og dens pKa, og de to er relateret af Henderson-Hasslebalch-ligningen. Denne ligning er: pH \u003d pKa + log [A -] /[AH], hvor [AH] er koncentrationen af
Sådan bestemmes pH ud fra pKaStyrken af en syre måles ved både dens pH og dens pKa, og de to er relateret af Henderson-Hasslebalch-ligningen. Denne ligning er: pH \u003d pKa + log [A -] /[AH], hvor [AH] er koncentrationen af -
 Sådan beregnes en rumperimeterHvis du nogensinde er blevet sendt til dit værelse til straf, kunne du måske have gået sin omkreds ud af kedsomhed. Et objekts omkreds er måling af grænser for dets område. Ligesom at bestemme rume
Sådan beregnes en rumperimeterHvis du nogensinde er blevet sendt til dit værelse til straf, kunne du måske have gået sin omkreds ud af kedsomhed. Et objekts omkreds er måling af grænser for dets område. Ligesom at bestemme rume


