Orale peptider:En ny æra i lægemiddeludvikling
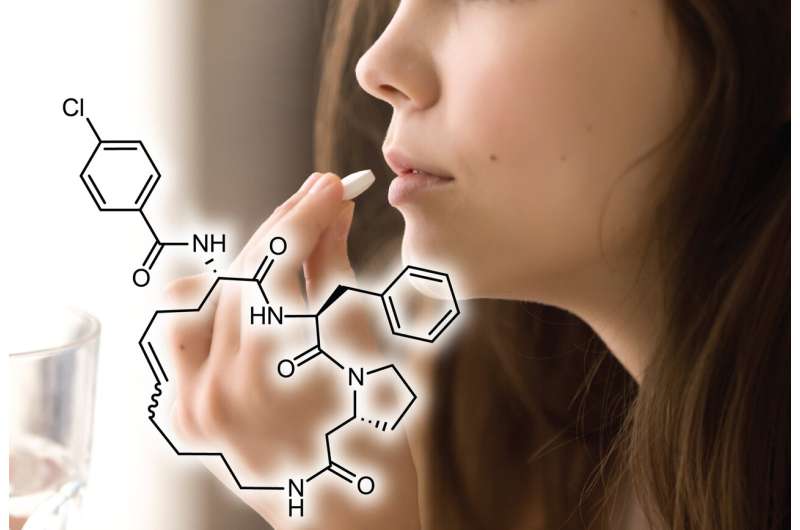
I årtier har et betydeligt antal proteiner, som er afgørende for behandling af forskellige sygdomme, forblevet undvigende for oral lægemiddelbehandling. Traditionelle små molekyler kæmper ofte for at binde til proteiner med flade overflader eller kræver specificitet for bestemte proteinhomologer. Typisk kræver større biologiske lægemidler, der kan målrette mod disse proteiner, injektion, hvilket begrænser patientens bekvemmelighed og tilgængelighed.
I en ny undersøgelse offentliggjort i Nature Chemical Biology, forskere fra professor Christian Heinis' laboratorium ved EPFL har opnået en betydelig milepæl inden for lægemiddeludvikling. Deres forskning åbner døren til en ny klasse af oralt tilgængelige lægemidler, der adresserer en langvarig udfordring i den farmaceutiske industri.
"Der er mange sygdomme, som målene blev identificeret for, men lægemidler, der binder og når dem, kunne ikke udvikles," siger Heinis. "De fleste af dem er kræfttyper, og mange mål i disse kræftformer er protein-protein-interaktioner, der er vigtige for tumorvæksten, men som ikke kan hæmmes."
Undersøgelsen fokuserede på cykliske peptider, som er alsidige molekyler kendt for deres høje affinitet og specificitet i binding af udfordrende sygdomsmål. Samtidig har det vist sig vanskeligt at udvikle cykliske peptider som oral medicin, fordi de hurtigt fordøjes eller absorberes dårligt af mave-tarmkanalen.
"Cycliske peptider er af stor interesse for udvikling af lægemidler, da disse molekyler kan binde sig til vanskelige mål, som det har været udfordrende at generere lægemidler til ved hjælp af etablerede metoder," siger Heinis. "Men de cykliske peptider kan normalt ikke administreres oralt - som en pille - hvilket begrænser deres anvendelse enormt."
Cykling-gennembrud
Forskerholdet målrettede enzymet thrombin, som er et kritisk sygdomsmål på grund af dets centrale rolle i blodkoagulationen; regulering af trombin er nøglen til at forebygge og behandle trombotiske lidelser som slagtilfælde og hjerteanfald.
For at generere cykliske peptider, der kan målrette thrombin og er tilstrækkeligt stabile, udviklede forskerne en to-trins kombinatorisk syntesestrategi til at syntetisere et stort bibliotek af cykliske peptider med thioetherbindinger, som øger deres metaboliske stabilitet, når de tages oralt.
"Vi er nu lykkedes med at generere cykliske peptider, der binder til et sygdomsmål efter vores valg, og som også kan administreres oralt," siger Heinis. "Til dette formål har vi udviklet en ny metode, hvor tusindvis af små cykliske peptider med tilfældige sekvenser syntetiseres kemisk på en nanoskala og undersøges i en high-throughput proces."
To trin, en gryde
Den nye metodeproces involverer to trin og foregår i den samme reaktive beholder, en funktion, som kemikere omtaler som "en gryde."
Det første trin er at syntetisere lineære peptider, som derefter gennemgår en kemisk proces, der danner en ringlignende struktur - i tekniske termer bliver "cykliseret." Dette gøres ved at bruge "bis-elektrofile linkere" - kemiske forbindelser, der bruges til at forbinde to molekylære grupper sammen - for at danne stabile thioetherbindinger.
I den anden fase gennemgår de cykliserede peptider acylering, en proces, der binder carboxylsyrer til dem, hvilket yderligere diversificerer deres molekylære struktur.
Teknikken eliminerer behovet for mellemliggende oprensningstrin, hvilket giver mulighed for high-throughput screening direkte i syntesepladerne, der kombinerer syntesen og screeningen af tusindvis af peptider for at identificere kandidater med høj affinitet for specifikke sygdomsmål - i dette tilfælde thrombin.
Ved hjælp af metoden er ph.d. studerende, der leder projektet, Manuel Merz, var i stand til at generere et omfattende bibliotek af 8.448 cykliske peptider med en gennemsnitlig molekylmasse på omkring 650 Dalton (Da), kun lidt over den maksimale grænse på 500 Da anbefalet for oralt tilgængelige små molekyler.
De cykliske peptider viste også en høj affinitet for thrombin.
Når de blev testet på rotter, viste peptiderne oral biotilgængelighed op til 18%, hvilket betyder, at når det cykliske peptidlægemiddel tages oralt, kommer 18% af det med succes ind i blodbanen og har en terapeutisk effekt. I betragtning af, at oralt administrerede cykliske peptider generelt udviser en biotilgængelighed på under 2 %, er en forøgelse af dette tal til 18 % et væsentligt fremskridt for lægemidler i kategorien biologiske lægemidler – som inkluderer peptider.
Indstilling af mål
Ved at muliggøre oral tilgængelighed af cykliske peptider har teamet åbnet muligheder for at behandle en række sygdomme, som har været udfordrende at håndtere med konventionelle orale lægemidler. Metodens alsidighed betyder, at den kan tilpasses til at målrette en bred vifte af proteiner, hvilket potentielt kan føre til gennembrud på områder, hvor medicinske behov i øjeblikket ikke er opfyldt.
"For at anvende metoden til mere udfordrende sygdomsmål, såsom protein-protein-interaktioner, vil større biblioteker sandsynligvis skulle syntetiseres og studeres," siger Manuel Merz. "Ved at automatisere yderligere trin af metoderne ser biblioteker med mere end en million molekyler ud til at være inden for rækkevidde."
I næste trin af dette projekt vil forskerne målrette mod adskillige intracellulære protein-protein-interaktionsmål, som det har været vanskeligt at udvikle inhibitorer for baseret på klassiske små molekyler. De er sikre på, at oralt anvendelige cykliske peptider kan udvikles til i det mindste nogle af dem.
Flere oplysninger: Alexander L. Nielsen, De novo udvikling af små cykliske peptider, der er oralt biotilgængelige, Nature Chemical Biology (2023). DOI:10.1038/s41589-023-01496-y
Journaloplysninger: Kemisk naturbiologi
Leveret af Ecole Polytechnique Federale de Lausanne
Sidste artikelNy strategi stabiliserer zink-ion-batterier
Næste artikelPiezoelektrisk-forstærkede p-n-kryds i fotoelektrokemiske systemer
 Varme artikler
Varme artikler
-
 Bløde dobbeltgyroider er unikke, men ufuldkommen, krystallerRice University materialeforsker Ned Thomas har en model af den blokcopolymer, han og hans laboratorium skabte for at se, om de kubiske strukturer indeni var perfekte eller ej. Undersøgelse med et ele
Bløde dobbeltgyroider er unikke, men ufuldkommen, krystallerRice University materialeforsker Ned Thomas har en model af den blokcopolymer, han og hans laboratorium skabte for at se, om de kubiske strukturer indeni var perfekte eller ej. Undersøgelse med et ele -
 En silica nanostruktur med kemo-enzymatisk opdelingElektronmikrografer af SiJAR (til venstre), elektronmikrografer og fluorescensmikrografer af SiJAR-injicerede celler (til højre). Kredit:POSTECH Da COVID-19-vaccinationer er godt i gang, mennesker
En silica nanostruktur med kemo-enzymatisk opdelingElektronmikrografer af SiJAR (til venstre), elektronmikrografer og fluorescensmikrografer af SiJAR-injicerede celler (til højre). Kredit:POSTECH Da COVID-19-vaccinationer er godt i gang, mennesker -
 Nanopartikelsensor kan skelne mellem viral og bakteriel lungebetændelseKredit:Unsplash/CC0 Public Domain Mange forskellige typer bakterier og vira kan forårsage lungebetændelse, men der er ingen nem måde at afgøre, hvilken mikrobe der forårsager en bestemt patients sy
Nanopartikelsensor kan skelne mellem viral og bakteriel lungebetændelseKredit:Unsplash/CC0 Public Domain Mange forskellige typer bakterier og vira kan forårsage lungebetændelse, men der er ingen nem måde at afgøre, hvilken mikrobe der forårsager en bestemt patients sy -
 Fremstilling af lysaktiverede proteinerRaziye Karapinar (til venstre) og Stefan Herlitze Kredit:RUB, Kramer En ny strategi til design af lysfølsomme proteiner er blevet udviklet af forskere ved Ruhr-Universität Bochum (RUB). Sådanne pr
Fremstilling af lysaktiverede proteinerRaziye Karapinar (til venstre) og Stefan Herlitze Kredit:RUB, Kramer En ny strategi til design af lysfølsomme proteiner er blevet udviklet af forskere ved Ruhr-Universität Bochum (RUB). Sådanne pr
- Gør vindmølleparker mere effektive
- Asteroidebyge på Jord-Måne-systemet for 800 millioner år siden afsløret af månekratere
- Forskere bygger en partikelaccelerator, der passer på en chip
- Hedebølger kan forårsage 10 gange mere afgrødeskader end nu anslået
- Verdensomspændende ransomware-cyberangreb:Hvad vi ved
- Forskning bekræfter visdommen i julemandens ønskelister, og viser, at feriehandlende ofte ikke kø…


