Bestem den idealiserede bindingsvinkel for OF2?
OF2 har et centralt oxygenatom bundet til to fluoratomer. Oxygenatomet har seks valenselektroner, og hvert fluoratom har syv valenselektroner.
1) Tæl det samlede antal valenselektroner:6 (O) + 2(7 F) =20 valenselektroner.
2) Bestem elektronpargeometrien:For at fordele disse 20 valenselektroner skal vi først have fire bindingspar af elektroner (to for hver binding) og derefter et ensomt par på oxygenatomet. Disse fem elektronpar vil have en trigonal bipyramidal elektronpargeometri.
3) Bestem den molekylære geometri:Den molekylære geometri afhænger af positionerne af de bundne atomer og enlige par. Det enlige par på iltatomet vil indtage en af de ækvatoriale positioner, mens de to fluoratomer vil indtage aksiale positioner for at minimere frastødningen mellem dem og det enlige par. Dette giver OF2 en bøjet molekylær geometri.
4) Forudsige den idealiserede bindingsvinkel:Den ideelle bindingsvinkel i en trigonal bipyramidal elektronpargeometri er 180 grader. Da et ensomt par indtager en ækvatorial position, vil bindingsvinklen mellem fluoratomerne blive komprimeret, og den idealiserede bindingsvinkel for OF2 vil være lidt mindre end 180 grader. Den nøjagtige bindingsvinkel kan bestemmes gennem eksperimentelle målinger eller beregningsmetoder og viser sig at være cirka 104 grader.
Sidste artikelHvilken type bjergart kan dannes ved kemiske reaktioner?
Næste artikelHvad er Ka for H2CO3 aq H HCO3 aq?
 Varme artikler
Varme artikler
-
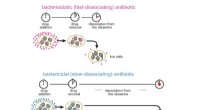 At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv
At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv -
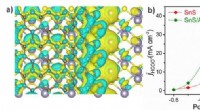 Forskere foreslår en ny strategi for elektrokemisk reduktion af kuldioxidDifferentialladningsdiagrammet for SnS/Aminated-C for (a) og den delvise strømtæthed af formiatproduktion for SnS og SnS/Aminated-C for (b). Kredit:CHEN Zhipeng Kuldioxid (CO 2 ) emission er ble
Forskere foreslår en ny strategi for elektrokemisk reduktion af kuldioxidDifferentialladningsdiagrammet for SnS/Aminated-C for (a) og den delvise strømtæthed af formiatproduktion for SnS og SnS/Aminated-C for (b). Kredit:CHEN Zhipeng Kuldioxid (CO 2 ) emission er ble -
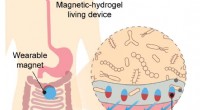 Levende sensorer undersøger tarmens mysterierSkematisk illustration af brugen af levende sensorer indkapslet i en magnetisk hydrogelanordning til undersøgelser af tarmen. Kredit:Xinyue Liu et al Forskning i den menneskelige tarm og mikrobe
Levende sensorer undersøger tarmens mysterierSkematisk illustration af brugen af levende sensorer indkapslet i en magnetisk hydrogelanordning til undersøgelser af tarmen. Kredit:Xinyue Liu et al Forskning i den menneskelige tarm og mikrobe -
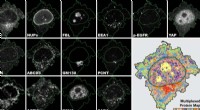 Ny metode forfiner celleprøveanalyse4i er den første billeddannelsesteknik, som giver os en multiplekset væv-til-organel-visning af biologiske prøver og forbinder flere oplysninger i et og samme eksperiment. Kredit:UZH Forskere ved
Ny metode forfiner celleprøveanalyse4i er den første billeddannelsesteknik, som giver os en multiplekset væv-til-organel-visning af biologiske prøver og forbinder flere oplysninger i et og samme eksperiment. Kredit:UZH Forskere ved
- Sådan tolk hierarkisk regression
- Hvad er konvergerende, divergerende og transformerende grænser?
- Smarte håndpumper forudsiger dybder af grundvand i Afrika
- Efterligning af natur på nanoskala:Selektiv transport over en biomimetisk nanopore
- Fransk domstol akserer markedsgodkendelse af Bayers Roundup ukrudtsdræber
- Forskere perfektionerer knudebindingsteknikker med molekylær streng


