Hvor mange elektroner er der i den ydre skal?
Her er en generel regel til bestemmelse af antallet af elektroner i den ydre skal af et atom baseret på dets position i det periodiske system:
1. Gruppe 1 grundstoffer (alkalimetaller):1 elektron i den ydre skal
2. Gruppe 2 grundstoffer (jordalkalimetaller):2 elektroner i den ydre skal
3. Gruppe 13 grundstoffer (borgruppe):3 elektroner i den ydre skal
4. Gruppe 14 grundstoffer (kulstofgruppe):4 elektroner i den ydre skal
5. Gruppe 15 grundstoffer (nitrogengruppe):5 elektroner i den ydre skal
6. Gruppe 16 grundstoffer (iltgruppe):6 elektroner i den ydre skal
7. Gruppe 17 grundstoffer (halogener):7 elektroner i den ydre skal
8. Gruppe 18 grundstoffer (ædelgasser):8 elektroner i den ydre skal (undtagen helium, som har 2 elektroner i den ydre skal)
Disse tal svarer til grundstoffets gruppenummer i det periodiske system. For eksempel har grundstoffer i gruppe 1 (alkalimetaller) én elektron i deres ydre skal, mens grundstoffer i gruppe 7 (halogener) har syv elektroner i deres ydre skal.
Det er vigtigt at bemærke, at denne regel kun gælder for hovedgruppeelementerne (Gruppe 1 til 18) og ikke inkluderer overgangsmetaller, som har en mere kompleks elektronkonfiguration.
Sidste artikelHvor mange elektroner er den ydre skal af klor?
Næste artikelHvor mange elektroner har nitrogen og brom i den ydre skal?
 Varme artikler
Varme artikler
-
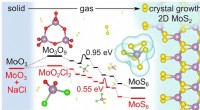 Undersøgelsesdetaljer, hvorfor 2D-molybdændisulfiddannelse får et hastighedsboost fra saltAlmindelig salt (NaCl) fungerer som et mellemled i den kemiske dampaflejringsvækst af 2D molybdændisulfid, hvilket fremskynder processen med dets skabelse. Materialeteoretikere ved Rice University opd
Undersøgelsesdetaljer, hvorfor 2D-molybdændisulfiddannelse får et hastighedsboost fra saltAlmindelig salt (NaCl) fungerer som et mellemled i den kemiske dampaflejringsvækst af 2D molybdændisulfid, hvilket fremskynder processen med dets skabelse. Materialeteoretikere ved Rice University opd -
 Kontrolleret dynamik af kolloide stængerModel af kolloide stænger af forskellig længde, som bevæger sig som skakbrikker på en magnetiseret chip. Kredit:Adrian Ernst. Kolloide partikler er blevet stadig vigtigere for forskning som bærere
Kontrolleret dynamik af kolloide stængerModel af kolloide stænger af forskellig længde, som bevæger sig som skakbrikker på en magnetiseret chip. Kredit:Adrian Ernst. Kolloide partikler er blevet stadig vigtigere for forskning som bærere -
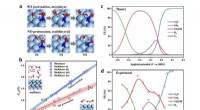 Forskere afslører potentiel afhængighed af nitrogenoxid -elektrisk reduktion til ammoniak(a)-(b) Verifikation af monolagsvandmodel i elektrokatalytiske energibarriereberegninger; (c)-(d) Sammenligning af teoretisk og eksperimentel faradaisk effektivitet. Kredit:LONG Jun Kvælstofoxid (
Forskere afslører potentiel afhængighed af nitrogenoxid -elektrisk reduktion til ammoniak(a)-(b) Verifikation af monolagsvandmodel i elektrokatalytiske energibarriereberegninger; (c)-(d) Sammenligning af teoretisk og eksperimentel faradaisk effektivitet. Kredit:LONG Jun Kvælstofoxid ( -
 Forskere udvikler ny behandling for knogleinfektion ved hjælp af kobberrigt glasimplantatUndersøgelsens første forfatter Emily Ryan, en nyligt kvalificeret ph.d.-studerende i RCSI Institut for Anatomi, afbilledet med prof Fergal OBrien, Professor i bioingeniør og regenerativ medicin i RCS
Forskere udvikler ny behandling for knogleinfektion ved hjælp af kobberrigt glasimplantatUndersøgelsens første forfatter Emily Ryan, en nyligt kvalificeret ph.d.-studerende i RCSI Institut for Anatomi, afbilledet med prof Fergal OBrien, Professor i bioingeniør og regenerativ medicin i RCS
- Sammenfiltring af fotoner af forskellige farver
- I fiktion, unge vælger traditionel kærlighed og kønsstereotyper
- Hvordan ser Albert Einstein ud?
- Forskere måler alt det stjernelys, der nogensinde er produceret af det observerbare univers
- Forskere udvikler strækbar trådformet superkondensator
- Sådan bliver du flypilot


