Hvad er hydroxid?
Hydroxid er en stærk base og et kraftigt oxidationsmiddel. Det er ætsende for metaller og kan forårsage forbrændinger på hud og væv. Hydroxid findes i mange husholdningsrengøringsprodukter, såsom afløbsrens og ovnrens. Det bruges også til produktion af papir, tekstiler og lægemidler.
I vand er hydroxidioner i ligevægt med hydrogenioner ifølge følgende ligning:
H2O ⇌ OH- + H+
Ligevægtskonstanten for denne reaktion kaldes vandets ioniseringskonstant , og den har en værdi på 1,0 × 10^-14 ved 25 °C. Det betyder, at koncentrationen af hydroxidioner i rent vand er meget lav, men den stiger i takt med at temperaturen stiger.
Koncentrationen af hydroxidioner i en opløsning kan måles ved hjælp af et pH-meter . En opløsnings pH er et mål for dens surhed eller basicitet, og den bestemmes af koncentrationen af hydrogenioner. En opløsning med en pH på 7 er neutral, en opløsning med en pH under 7 er sur, og en opløsning med en pH over 7 er basisk.
Hydroxidioner er vigtige i mange biologiske processer. De er involveret i reguleringen af pH, transporten af næringsstoffer og syntesen af proteiner. Hydroxidioner er også essentielle for aktiviteten af mange enzymer.
 Varme artikler
Varme artikler
-
 Skræddersyet kulstof kan hjælpe forskere med at finde arvelige sygdomme og de rigtige doser af med…Den nye metode gør det muligt at opdele det eksperimentelle spektrum produceret ved røntgenspektroskopi i data på atomniveau. Kredit:Anja Aarva / Aalto University Sensorer fremstillet med kulstofb
Skræddersyet kulstof kan hjælpe forskere med at finde arvelige sygdomme og de rigtige doser af med…Den nye metode gør det muligt at opdele det eksperimentelle spektrum produceret ved røntgenspektroskopi i data på atomniveau. Kredit:Anja Aarva / Aalto University Sensorer fremstillet med kulstofb -
 Test af designet kulstofmaterialer til at rense spildevandKredit:CC0 Public Domain Affaldsstrømme fra industri og landbrug kunne bruges til produktion af kul, der kan tjene som en billig adsorbent til vandrensning. I sit speciale på Industridoktoralskole
Test af designet kulstofmaterialer til at rense spildevandKredit:CC0 Public Domain Affaldsstrømme fra industri og landbrug kunne bruges til produktion af kul, der kan tjene som en billig adsorbent til vandrensning. I sit speciale på Industridoktoralskole -
 Polymer termisk regulator omdannes fra leder til isolator og tilbage igenDen rotationsforstyrrede sekskantede fase. Kredit:College of Engineering Polymerer bruges til at udvikle forskellige materialer, såsom plastik, nylon og gummi. I deres mest grundlæggende form, de
Polymer termisk regulator omdannes fra leder til isolator og tilbage igenDen rotationsforstyrrede sekskantede fase. Kredit:College of Engineering Polymerer bruges til at udvikle forskellige materialer, såsom plastik, nylon og gummi. I deres mest grundlæggende form, de -
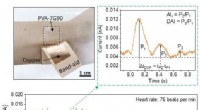 Opfindelsen tilbyder en ny mulighed for overvågning af hjertesundhedEt team fra Purdue University udviklede selvdrevne bærbare triboelektriske nanogeneratorer med polyvinylalkohol-baserede kontaktlag til overvågning af kardiovaskulær sundhed. Kredit:Wenzhuo Wu/Purdue
Opfindelsen tilbyder en ny mulighed for overvågning af hjertesundhedEt team fra Purdue University udviklede selvdrevne bærbare triboelektriske nanogeneratorer med polyvinylalkohol-baserede kontaktlag til overvågning af kardiovaskulær sundhed. Kredit:Wenzhuo Wu/Purdue
- Potentielt store økonomiske konsekvenser af klimaændringer kan undgås ved menneskelige handlinger
- Er hydrogen en fast væske eller gas?
- Jordens magnetiske skjold boomer som en tromle, når den rammes af impulser
- En ny måde at forbedre hukommelsesenhedernes kapacitet på
- Forbedring af undervisningskvalitet gennem kvalitativ feedback... ved hjælp af maskiner
- G20 digital skat kommer et skridt nærmere


