Hvad har natriumhydroxid og kalium til fælles?
Der er dog også nogle vigtige forskelle mellem natriumhydroxid og kalium. Natriumhydroxid er en meget opløselig forbindelse, hvilket betyder, at den let opløses i vand. I modsætning hertil er kalium et moderat opløseligt metal, der kun delvist opløses i vand. Denne forskel i opløselighed påvirker reaktiviteten af disse stoffer. Natriumhydroxid er mere reaktivt end kalium i vand, fordi dets ioner er lettere tilgængelige til at deltage i kemiske reaktioner.
Derudover er natriumhydroxid en stærkere base end kalium. Det betyder, at det har en højere tendens til at donere elektroner eller hydroxidioner (OH-) i vand, hvilket resulterer i et højere pH-niveau. Kalium er på den anden side en svagere base og har en lavere tendens til at donere elektroner, hvilket fører til et lavere pH-niveau.
Samlet set er natriumhydroxid og kalium begge meget reaktive elementer, der undergår hydrolyse, når de kommer i kontakt med vand, frigiver varme og danner en base. Imidlertid resulterer deres forskelle i opløselighed og basicitet i variationer i deres reaktivitet og styrken af de resulterende baser.
Sidste artikelHvordan opløses jorden i vand?
Næste artikelHvad er mere farligt koncentreret alkali eller fortyndet alkali?
 Varme artikler
Varme artikler
-
 Ny teknik kunne fremskynde produktionen af affald til metanKandidatstuderende i miljøteknik Bappi Chowdhury (til venstre) og vejleder Bipro Dhar i laboratoriet med en fordøjetank, de er ved at udvikle, der bruger mikrober til at omdanne en blanding af madaffa
Ny teknik kunne fremskynde produktionen af affald til metanKandidatstuderende i miljøteknik Bappi Chowdhury (til venstre) og vejleder Bipro Dhar i laboratoriet med en fordøjetank, de er ved at udvikle, der bruger mikrober til at omdanne en blanding af madaffa -
 Hærens nye fund sænker utilsigtet detonation af lagreLaser-induceret plasma:Snapshots fra højhastighedsvideo, der viser dannelsen af et laser-induceret plasma (8,9 mm højt) på en eksplosiv rest; den resulterende chokbølge vises i det første billede. K
Hærens nye fund sænker utilsigtet detonation af lagreLaser-induceret plasma:Snapshots fra højhastighedsvideo, der viser dannelsen af et laser-induceret plasma (8,9 mm højt) på en eksplosiv rest; den resulterende chokbølge vises i det første billede. K -
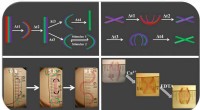 4-D bioingeniørmaterialer bøjning, kurve som naturligt væv4D hydrogel-baserede materialer kan gennemgå flere konformationelle formændringer som reaktion på miljømæssige signaler. Kredit:Aixiang Ding Vævsteknik har længe været afhængig af geometrisk stati
4-D bioingeniørmaterialer bøjning, kurve som naturligt væv4D hydrogel-baserede materialer kan gennemgå flere konformationelle formændringer som reaktion på miljømæssige signaler. Kredit:Aixiang Ding Vævsteknik har længe været afhængig af geometrisk stati -
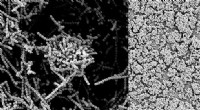 Sukker i modermælk er en ny klasse af antibakterielle midlerNærbilledet til venstre illustrerer, hvordan Strep-bakterier normalt klumper sig sammen for at danne en beskyttende biofilm. Billedet til højre viser, at biofilmen nedbrydes, når en Strep-kultur doser
Sukker i modermælk er en ny klasse af antibakterielle midlerNærbilledet til venstre illustrerer, hvordan Strep-bakterier normalt klumper sig sammen for at danne en beskyttende biofilm. Billedet til højre viser, at biofilmen nedbrydes, når en Strep-kultur doser


