Hvad sker der med jern, når det reagerer med kobbersulfat?
1. Dannelse af jernsulfat:
Jern (Fe) atomer fra jernmetallet reagerer med sulfationerne (SO4^2-) fra kobbersulfat, hvilket resulterer i dannelsen af jernsulfat (FeSO4). Denne forbindelse er opløselig i vand og producerer en grøn-farvet opløsning.
2. Forskydning af kobber:
Når jernatomerne fortrænger kobberionerne (Cu^2+) fra kobbersulfatforbindelsen, dannes metallisk kobber. Dette kobber aflejres på overfladen af jernmetallet som en rødbrun belægning.
3. Redox-reaktion:
Denne reaktion er et eksempel på en redoxreaktion, der involverer både oxidation og reduktion. Jern undergår oxidation, da dets oxidationstilstand ændres fra 0 (i elementært jern) til +2 (i jernsulfat). På den anden side gennemgår kobber reduktion, da dets oxidationstilstand falder fra +2 (i kobbersulfat) til 0 (i metallisk kobber).
Samlet reaktion:
Den overordnede kemiske ligning for reaktionen kan skrives som:
Fe(s) + CuSO4(aq) → FeSO4(aq) + Cu(s)
Sammenfattende, når jern reagerer med kobbersulfat, dannes jernsulfat og metallisk kobber. Jernatomerne erstatter kobberatomer i kobbersulfat, hvilket fører til dannelsen af en grønfarvet jernsulfatopløsning og en rødbrun kobberbelægning på jernmetallet.
 Varme artikler
Varme artikler
-
 Kan jeg blande disse kemikalier? Der er en app til det!En visuel fremstilling, der viser, hvordan tildeling af graffarveregistre fungerer. Kredit:Jason Ott/UCR Forkert blandede kemikalier forårsager et chokerende antal brande, eksplosioner, og skader
Kan jeg blande disse kemikalier? Der er en app til det!En visuel fremstilling, der viser, hvordan tildeling af graffarveregistre fungerer. Kredit:Jason Ott/UCR Forkert blandede kemikalier forårsager et chokerende antal brande, eksplosioner, og skader -
 Varme klogere, ikke sværere:Hvordan mikrobølger gør katalytiske reaktioner mere effektiveKonventionel opvarmning kontra mikrobølgeopvarmning. Kredit:Tokyo Institute of Technology Mange reaktioner, som vi bruger til at producere kemiske forbindelser i fødevarer, medicinsk, og industrie
Varme klogere, ikke sværere:Hvordan mikrobølger gør katalytiske reaktioner mere effektiveKonventionel opvarmning kontra mikrobølgeopvarmning. Kredit:Tokyo Institute of Technology Mange reaktioner, som vi bruger til at producere kemiske forbindelser i fødevarer, medicinsk, og industrie -
 Fysikere måler molekylære elektroniske egenskaber af vitaminerDenne kunstners syn på eksperimentet illustrerer, at naturligt forekommende vitaminer kan fremstilles i specifikke kvantetilstande, der letter måling af de molekylære elektroniske egenskaber. Kredit:C
Fysikere måler molekylære elektroniske egenskaber af vitaminerDenne kunstners syn på eksperimentet illustrerer, at naturligt forekommende vitaminer kan fremstilles i specifikke kvantetilstande, der letter måling af de molekylære elektroniske egenskaber. Kredit:C -
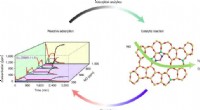 Ingeniører løser mysteriet om struktur-egenskabsforhold i emissionskontrolkatalysatorerGrafisk abstrakt. Kredit: Naturkatalyse (2021). DOI:10.1038/s41929-020-00555-0 Miljøbevarelse og fremtidig bæredygtighed kræver innovation fra kemiingeniører, fra justeringer til den mikroskopisk
Ingeniører løser mysteriet om struktur-egenskabsforhold i emissionskontrolkatalysatorerGrafisk abstrakt. Kredit: Naturkatalyse (2021). DOI:10.1038/s41929-020-00555-0 Miljøbevarelse og fremtidig bæredygtighed kræver innovation fra kemiingeniører, fra justeringer til den mikroskopisk
- Curiosity tester en ny måde at bore på Mars
- Forbindelse fundet mellem Arktisk Oscillation og øget risiko for brand i Sibirien
- Sporing af vand fra flod til akvifer
- Hvordan en vulkan og flammende røde solnedgange fik en amatørforsker på Hawaii til at opdage jets…
- Løsning af de forhindringer, der forhindrer kommercialiseringen af lithiumrige lagdelte sulfider
- Ræv, Comcast byder på Sky i sjældne auktioner


