Hvis 3,21 mol af en gas optager 56,2 L ved 44 C og 793 torr 5,29 L, optager dette?
```
PV =nRT
```
Hvor:
* P er trykket i atmosfæren
* V er volumen i liter
* n er antallet af mol gas
* R er den ideelle gaskonstant (0,08206 L * atm / mol * K)
* T er temperaturen i Kelvin
Vi får følgende oplysninger:
* n =3,21 mol
* V =56,2 L
* T =44 °C + 273,15 =317,15 K
* P =793 torr * (1 atm / 760 torr) =1,043 atm
Vi kan omarrangere den ideelle gaslov til at løse for V:
```
V =nRT/P
```
Ved at erstatte vores værdier i får vi:
```
V =(3,21 mol * 0,08206 L * atm/mol * K * 317,15 K) / 1,043 atm
```
```
V =84,5 L
```
Derfor fylder gassen 84,5 L under de givne forhold.
Sidste artikelSuser marmor i saltsyre?
Næste artikelHvordan forsurer man jorden?
 Varme artikler
Varme artikler
-
 Nanokrystallinske materialer med reduceret ilt viser forbedret ydeevnePostdoktorforsker Peiman Shahbegi-Roodposhti og en bachelorstuderende i materialevidenskab arbejder med en handskekasse for at producere nanomaterialer. Kredit:University of Connecticut Forskere v
Nanokrystallinske materialer med reduceret ilt viser forbedret ydeevnePostdoktorforsker Peiman Shahbegi-Roodposhti og en bachelorstuderende i materialevidenskab arbejder med en handskekasse for at producere nanomaterialer. Kredit:University of Connecticut Forskere v -
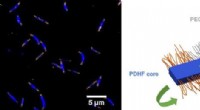 Polymer krystaller er nøglen til rekordstor energitransportBillede, der viser lysemission fra de polymere nanostrukturer og skematisk af en enkelt nanostruktur. Kredit:University of Bristol Forskere fra universiteterne i Bristol og Cambridge har fundet en
Polymer krystaller er nøglen til rekordstor energitransportBillede, der viser lysemission fra de polymere nanostrukturer og skematisk af en enkelt nanostruktur. Kredit:University of Bristol Forskere fra universiteterne i Bristol og Cambridge har fundet en -
 Ny teknologi fuldender vital klasse af industrielle reaktioner fem gange hurtigereNUS-forskerteamet ledet af Assoc Prof Yan Ning (midten) brugte en elektrostationsmaskine til at opnå den ønskede oscillation af elektriske potentialer for at fremskynde hydrogeneringen i en reaktor i
Ny teknologi fuldender vital klasse af industrielle reaktioner fem gange hurtigereNUS-forskerteamet ledet af Assoc Prof Yan Ning (midten) brugte en elektrostationsmaskine til at opnå den ønskede oscillation af elektriske potentialer for at fremskynde hydrogeneringen i en reaktor i -
 Spiropyran-funktionaliserede fotokromiske nylonbånd til langtidsføling af ultraviolet lys(a) Snapshots af SP-funktionaliserede webbings over otte ugers UV-eksponering. (b) Tidsmæssig udvikling af webbingsets farve repræsenteret i CIE 1976-farverummet. Indsatsen er en zoomet visning, og de
Spiropyran-funktionaliserede fotokromiske nylonbånd til langtidsføling af ultraviolet lys(a) Snapshots af SP-funktionaliserede webbings over otte ugers UV-eksponering. (b) Tidsmæssig udvikling af webbingsets farve repræsenteret i CIE 1976-farverummet. Indsatsen er en zoomet visning, og de
- Juno esses ottende videnskabspas af Jupiter
- Sibiriens permafrosterosion er blevet forværret i årevis
- En ny matematisk tilgang til forståelse af zeolitter
- Hvad skete der før, under og efter dannelsen af solsystemet? Asteroid Ryugu-undersøgelsen indeho…
- Sahara -ørkenen udvider sig - verdens største ørken voksede med 10 procent siden 1920
- NASA sætter fokus på lanceringen af InSight Mars-missionen den 5. maj


