Når en prøve på 20,0 g CoCl2 - 6H2O tørres i en ovn indtil tør opnået, hvad massen koboltchlorid?
Formlen for cobaltchloridhexahydrat angiver, at der er seks vandmolekyler forbundet med hver formelenhed af CoCl2. Når de opvarmes, bliver disse vandmolekyler drevet af som damp og efterlader det vandfri koboltchlorid.
Den molære masse af CoCl2 - 6H2O er 237,93 g/mol, mens den molære masse af vandfri CoCl2 er 129,84 g/mol.
For at beregne massen af CoCl2 i den originale prøve kan vi opsætte en andel baseret på molforholdet mellem CoCl2 og CoCl2 - 6H2O:
(Masse af CoCl2) / (Molar masse af CoCl2) =(Masse af CoCl2 - 6H2O) / (Molar masse af CoCl2 - 6H2O)
Erstatning af de givne værdier:
(Masse af CoCl2) / 129,84 g/mol =20,0 g / 237,93 g/mol
Løsning for massen af CoCl2:
Masse af CoCl2 =(129,84 g/mol) * (20,0 g / 237,93 g/mol)
=10,98 g
Derfor er massen af cobaltchlorid opnået efter tørring af 20,0 g prøven af CoCl2 - 6H2O ca. 10,98 g.
 Varme artikler
Varme artikler
-
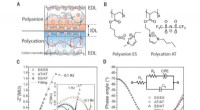 Ionotronisk teknologi, der ikke kræver flydende elektrolytterDannelse af en IDL ved grænsefladen mellem to modsat ladede ionoelastomerer. (A) Skematisk illustration af en polyanion/polykation-forbindelse. Kulstof-nanorørelektroder med stort overfladeareal er in
Ionotronisk teknologi, der ikke kræver flydende elektrolytterDannelse af en IDL ved grænsefladen mellem to modsat ladede ionoelastomerer. (A) Skematisk illustration af en polyanion/polykation-forbindelse. Kulstof-nanorørelektroder med stort overfladeareal er in -
 Nedbrydningsstatus for moderne polymere museumsartefakter kan klassificeres efter deres lugtKredit:Wiley Åndedrætsanalyse i sygdomsdiagnostik er et lovende forskningsfelt, og fremskridtene inden for instrumentering muliggør nøjagtig påvisning af metabolitter. Men ikke kun patienternes he
Nedbrydningsstatus for moderne polymere museumsartefakter kan klassificeres efter deres lugtKredit:Wiley Åndedrætsanalyse i sygdomsdiagnostik er et lovende forskningsfelt, og fremskridtene inden for instrumentering muliggør nøjagtig påvisning af metabolitter. Men ikke kun patienternes he -
 Forskere identificerer enzym, der er ansvarligt for at hjælpe kræfttumorer med at sprede sigSteven Van Doren afslørede, hvordan et kræftkritisk enzym er placeret på celleoverflader. Kredit:University of Missouri-Columbia Forskere ved University of Missouri har opdaget, hvordan et kræftkr
Forskere identificerer enzym, der er ansvarligt for at hjælpe kræfttumorer med at sprede sigSteven Van Doren afslørede, hvordan et kræftkritisk enzym er placeret på celleoverflader. Kredit:University of Missouri-Columbia Forskere ved University of Missouri har opdaget, hvordan et kræftkr -
 Ny sensor kan snart teste for coronavirus og influenza samtidigtDenne sensor er på størrelse med et mikro-USB-drev og er i stand til at teste for influenza og COVID-19 samtidigt. Kredit:Dmitry Kireev, University of Texas i Austin Den nye coronavirus er blevet
Ny sensor kan snart teste for coronavirus og influenza samtidigtDenne sensor er på størrelse med et mikro-USB-drev og er i stand til at teste for influenza og COVID-19 samtidigt. Kredit:Dmitry Kireev, University of Texas i Austin Den nye coronavirus er blevet
- Er kobber et metal ikke-metal eller metalloid?
- Jorden filtrerer nogle nye forurenende stoffer fra, før den når grundvandet
- Lockheed Vega
- Nvidia køber den israelske chipproducent Mellanox for $6,9 mia
- Hvordan kan rådgivere adressere social retfærdighed midt i klimaforandringerne?
- Hvor meget regnskov har fugle brug for?


