Hvad er kerneelektroner i Cobalts -elektronkonfiguration?
1. Elektronkonfiguration af kobolt:
Cobalt (CO) har et atomnummer på 27, hvilket betyder, at det har 27 elektroner. Dens elektronkonfiguration er:
* 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3d⁷
2. Identificering af kerneelektroner:
* kerneelektroner er elektronerne i de indre skaller af et atom. De er ikke involveret i kemisk binding.
* valenselektroner er elektronerne i den yderste skal. De er involveret i kemisk binding.
3. Bestemmelse af kerneelektroner til kobolt:
* De første tre skaller (1S², 2S² 2P⁶, 3S² 3P⁶) betragtes som kerneelektroner.
* 4S² og 3D⁷ -elektronerne er valenselektroner.
Derfor er kerneelektroner i Cobalts elektronkonfiguration:
* 1S² 2S² 2P⁶ 3S² 3P⁶
Sidste artikelHvad er en anden metode til at adskille blandingen i kemi?
Næste artikelHvad er forholdet mellem kuldioxid og glukose?
 Varme artikler
Varme artikler
-
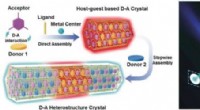 Heterostrukturkrystaller kunne lyse vejen til optiske kredsløbKredit:Wiley-VCH Det kan være muligt at nå nye niveauer af miniaturisering, hastighed, og databehandling med optiske kvantecomputere, som bruger lys til at transportere information. For det, vi ha
Heterostrukturkrystaller kunne lyse vejen til optiske kredsløbKredit:Wiley-VCH Det kan være muligt at nå nye niveauer af miniaturisering, hastighed, og databehandling med optiske kvantecomputere, som bruger lys til at transportere information. For det, vi ha -
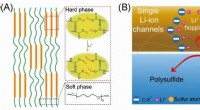 Stabiliserende svovlkatode med enkelt Li-ion-kanal polymerbindemiddel(A) Skematiske diagrammer over dannelsen af polymeren med enkeltionkanalerne. (B) Skematiske diagrammer af enkelt-ion-kanaler regulerer polysulfid- og Li-ion-hopningen. Kredit:©Science China Press
Stabiliserende svovlkatode med enkelt Li-ion-kanal polymerbindemiddel(A) Skematiske diagrammer over dannelsen af polymeren med enkeltionkanalerne. (B) Skematiske diagrammer af enkelt-ion-kanaler regulerer polysulfid- og Li-ion-hopningen. Kredit:©Science China Press -
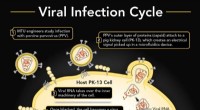 Microfluidics hjælper ingeniører med at se virusinfektion i realtid1. Porcint parvovirus (PPV) inficerer en svinenyrecelle (PK-13). 2. PPV binder sig til PK-13 ved hjælp af dets ydre lag af proteiner (kapsid), som kan detekteres i en mikrofluidikanordning. 3. Det vir
Microfluidics hjælper ingeniører med at se virusinfektion i realtid1. Porcint parvovirus (PPV) inficerer en svinenyrecelle (PK-13). 2. PPV binder sig til PK-13 ved hjælp af dets ydre lag af proteiner (kapsid), som kan detekteres i en mikrofluidikanordning. 3. Det vir -
 Hvor let kan et foldbart og langtidsholdbart batteri være?Viser fleksibilitet af en monolitisk organisk elektrode Kredit:Soojin Park(POSTECH) Med lanceringen af bærbare enheder og smartphones, der kræver en høj kapacitet af elektricitet, såsom foldbare
Hvor let kan et foldbart og langtidsholdbart batteri være?Viser fleksibilitet af en monolitisk organisk elektrode Kredit:Soojin Park(POSTECH) Med lanceringen af bærbare enheder og smartphones, der kræver en høj kapacitet af elektricitet, såsom foldbare


