Hvilke former ved katoden under elektrolyse af en metalforbindelse?
* det frie metal: Dette er det mest almindelige resultat. Metalionerne i opløsningen migrerer mod den negativt ladede katode, hvor de får elektroner og reduceres til deres elementære form. I elektrolysen af kobbersulfat (CUSO₄) reduceres kobberioner (Cu²⁺) for eksempel ved katoden for at danne fast kobbermetal (Cu).
* brintgas: Hvis metallet er mindre reaktivt end brint, reduceres brintioner (H⁺) fra opløsningen ved katoden i stedet for metalioner. Dette resulterer i udviklingen af brintgas (H₂). For eksempel produceres hydrogengas i elektrolysen af en opløsning indeholdende natriumchlorid (NaCI) ved katoden, mens natriumioner (Na⁺) forbliver i opløsning.
* Andre arter: Afhængig af den specifikke forbindelse og betingelser kan andre arter dannes ved katoden. Disse kan omfatte:
* hydratiserede metalioner: I nogle tilfælde reduceres metalioner muligvis ikke fuldt ud til den elementære tilstand, men danner hydratiserede metalioner.
* Metalliske legeringer: Hvis opløsningen indeholder flere metalioner, kan der dannes legeringer ved katoden.
Sammenfattende afhænger det specifikke produkt, der dannes ved katoden under elektrolyse, af den relative reaktivitet af metallet og brint såvel som de specifikke betingelser for elektrolysen.
 Varme artikler
Varme artikler
-
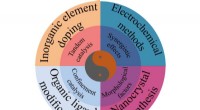 Tuningstrategier og struktureffekter af elektrokatalysatorer til kuldioxidreduktionsreaktionenForskellige afstemningsstrategier muliggør forskelle i katalysatorstrukturer. Hvordan træffer man et valg fra disse tilgængelige tuning-strategier? Der kan foretages en afvejning mellem den ønskede st
Tuningstrategier og struktureffekter af elektrokatalysatorer til kuldioxidreduktionsreaktionenForskellige afstemningsstrategier muliggør forskelle i katalysatorstrukturer. Hvordan træffer man et valg fra disse tilgængelige tuning-strategier? Der kan foretages en afvejning mellem den ønskede st -
 Ny stabil form for plutonium opdagetKredit:CC0 Public Domain Et internationalt team af forskere, ledet af Helmholtz Zentrum Dresden-Rossendorf (HZDR), har fundet en ny forbindelse af plutonium med en uventet, pentavalent oxidationst
Ny stabil form for plutonium opdagetKredit:CC0 Public Domain Et internationalt team af forskere, ledet af Helmholtz Zentrum Dresden-Rossendorf (HZDR), har fundet en ny forbindelse af plutonium med en uventet, pentavalent oxidationst -
 Forskere laver nye opskrifter til at tage salt ud af havvandKredit:CC0 Public Domain Mens befolkningerne boomer og kronisk tørke fortsætter, Kystbyer som Carlsbad i det sydlige Californien har i stigende grad vendt sig til havafsaltning for at supplere en
Forskere laver nye opskrifter til at tage salt ud af havvandKredit:CC0 Public Domain Mens befolkningerne boomer og kronisk tørke fortsætter, Kystbyer som Carlsbad i det sydlige Californien har i stigende grad vendt sig til havafsaltning for at supplere en -
 Hybride enzymkatalysatorer syntetiseret ved en de novo tilgang til udvidelse af biokatalyseKredit:Chinese Journal of Catalysis De to store udfordringer i industriel enzymatisk katalyse er det begrænsede antal kemiske reaktionstyper, der katalyseres af enzymer og ustabilitet af enzymer u
Hybride enzymkatalysatorer syntetiseret ved en de novo tilgang til udvidelse af biokatalyseKredit:Chinese Journal of Catalysis De to store udfordringer i industriel enzymatisk katalyse er det begrænsede antal kemiske reaktionstyper, der katalyseres af enzymer og ustabilitet af enzymer u
- Geologer producerer en ny tidslinje for Jordens paleozoiske klimaændringer
- Hvorfor er en basketball ikke konstrueret som massestruktur?
- NASA-billeder afslører Kujira i overgangen til en ekstratropisk cyklon
- Syreangreb – kan muslinger hænge ved meget længere?
- Reproduktion af planteceller
- Frekvensstabilisering i ikke -lineære nanomekaniske oscillatorer


