Hvis et produkt en kemisk reaktion fjernes, er reaktionen?
Her er hvorfor:
* le Chateliers princip: Dette princip siger, at hvis der anvendes en ændring af betingelsen på et system i ligevægt, vil systemet skifte i en retning, der lindrer stresset.
* stress: Fjernelse af et produkt er en stress på systemet.
* aflastning af stress: Systemet vil forsøge at erstatte det fjernede produkt ved at skifte ligevægt for at favorisere den fremadgående reaktion (reaktanter på produkter).
Eksempel:
Forestil dig en simpel reversibel reaktion:
a + b ⇌ c + d
Hvis produkt C fjernes, skifter systemet til højre og producerer mere C og D for at kompensere.
Vigtige overvejelser:
* ligevægt: Dette princip gælder for reaktioner i ligevægt. Hvis reaktionen endnu ikke har nået ligevægt, kan fjernelse af et produkt simpelthen bremse den samlede reaktionshastighed.
* reversibilitet: Reaktionen skal være reversibel for Le Chateliers princip at anvende.
* Andre faktorer: Andre faktorer som temperatur, tryk og katalysatorer kan også påvirke reaktionsbalancen.
Fortæl mig, hvis du gerne vil udforske specifikke eksempler eller andre aspekter af kemisk ligevægt!
Sidste artikelHvorfor har magnesiumsulfat ikke en LD50?
Næste artikelHvad er den pseudo ædle gasnotation af NA?
 Varme artikler
Varme artikler
-
 Ioniske edderkoppespind, der imiterer dobbelte funktioner i ægte edderkoppespindKredit:Unsplash/CC0 Public Domain Et team af forskere fra Seoul National University og Eumam Middle School har udviklet en type ionisk edderkoppespind, der er i stand til at efterligne dobbelte fu
Ioniske edderkoppespind, der imiterer dobbelte funktioner i ægte edderkoppespindKredit:Unsplash/CC0 Public Domain Et team af forskere fra Seoul National University og Eumam Middle School har udviklet en type ionisk edderkoppespind, der er i stand til at efterligne dobbelte fu -
 Udnyttelse af overskydende kuldioxidDette er bismuth. UD-forskere har identificeret en specialiseret kapacitet i metal, kaldet katalytisk plasticitet, ”, der kan udnyttes til at omdanne kuldioxid til flydende brændstoffer og industriell
Udnyttelse af overskydende kuldioxidDette er bismuth. UD-forskere har identificeret en specialiseret kapacitet i metal, kaldet katalytisk plasticitet, ”, der kan udnyttes til at omdanne kuldioxid til flydende brændstoffer og industriell -
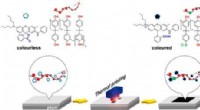 Et skridt i retning af at kvitte register kvitteringer af BPAKredit:American Chemical Society Selvom USA og andre lande har forbudt eller begrænset brugen af bisphenol A (BPA) på grund af miljø- og sundhedsmæssige bekymringer, det bruges stadig i termotry
Et skridt i retning af at kvitte register kvitteringer af BPAKredit:American Chemical Society Selvom USA og andre lande har forbudt eller begrænset brugen af bisphenol A (BPA) på grund af miljø- og sundhedsmæssige bekymringer, det bruges stadig i termotry -
 NIST præsenterer den første test i den virkelige verden af nye designs til røggasemissionerNIST designet to nye pitotprober (venstre og i midten), den ene, hvis sanseflade er kegleformet, og den anden, hvis overflade er halvkugleformet. Proberne har fem huller, eller havne. Sammenligning af
NIST præsenterer den første test i den virkelige verden af nye designs til røggasemissionerNIST designet to nye pitotprober (venstre og i midten), den ene, hvis sanseflade er kegleformet, og den anden, hvis overflade er halvkugleformet. Proberne har fem huller, eller havne. Sammenligning af
- Hvordan er fysik relateret til samfundsfag?
- Hvad er et ydre lag af gas, der på terrestrisk planet?
- Hvad er den gennemsnitlige hastighed, hvis et tog bevæger sig 225 kilometer på 2,5 timer?
- Sådan beregnes et område i kvadratmeter
- Vietnam fastholder forbud mod dybvandsfiskeri i forurenede områder
- Omformulering af den kontroversielle bushmeat-handel:Hvem bestemmer, hvilke fødevarer der er passen…


