Hvordan genkender du eksotermiske og endotermiske reaktioner?
eksotermiske reaktioner
* Energiudgivelse: Disse reaktioner frigiver energi i omgivelserne, normalt som varme.
* observerbare effekter:
* stigning i temperatur: Omgivelserne (som et bægerglas eller luften) føles varmere.
* Produktion af lys: Nogle eksoterme reaktioner producerer en flamme eller glød.
* Dannelse af et bundfald (fast): Dette kan undertiden forekomme som et resultat af energiudgivelsen.
* Eksempler:
* Brændende træ eller brændstof
* Eksplosioner
* Neutralisering af syrer og baser
* Forbrændingsreaktioner
endotermiske reaktioner
* Energiabsorption: Disse reaktioner absorberer energi fra omgivelserne.
* observerbare effekter:
* fald i temperatur: Omgivelserne føles koldere.
* opløsning af salte: Nogle salte, som ammoniumnitrat, absorberer varme, når de opløses i vand, hvilket får opløsningen til at føle sig kold.
* Eksempler:
* Fotosyntese
* Meltende is
* Madlavning af et æg
* Opløsning af nogle salte i vand
her er en nyttig måde at huske på:
* exo betyder "out" - eksotermiske reaktioner frigiver energi * ud * i omgivelserne.
* endo betyder "i" - endotermiske reaktioner tager energi * i * fra omgivelserne.
Vigtig note:
Mens temperaturændring er en almindelig indikator, er det ikke den eneste måde at genkende disse reaktioner på. Nogle eksoterme reaktioner har muligvis ikke en signifikant temperaturstigning, og nogle endotermiske reaktioner kan muligvis være drevet af andre faktorer som lysenergi.
Sidste artikelEr Venus lavet for det meste ude af klippe og gas?
Næste artikelHvad er densiteten af phenolformaldehydharpiks?
 Varme artikler
Varme artikler
-
 Forskere opdager nye strukturer i den mindste isterningForskere opdagede nye strukturer i den mindste isterning. Kredit:Li Gang og Li Qinming Nedfrysning af vand er en af de mest almindelige processer. Imidlertid, Det har været en udfordring at fors
Forskere opdager nye strukturer i den mindste isterningForskere opdagede nye strukturer i den mindste isterning. Kredit:Li Gang og Li Qinming Nedfrysning af vand er en af de mest almindelige processer. Imidlertid, Det har været en udfordring at fors -
 Organisk kationinterkalering:En effektiv strategi til manipulation af båndtopologi og superledningKredit:CC0 Public Domain I en nylig artikel offentliggjort i Videnskabsbulletin , forskere udviklede en effektiv organisk-kation-interkalationsstrategi til at manipulere mellemlagskoblingen af
Organisk kationinterkalering:En effektiv strategi til manipulation af båndtopologi og superledningKredit:CC0 Public Domain I en nylig artikel offentliggjort i Videnskabsbulletin , forskere udviklede en effektiv organisk-kation-interkalationsstrategi til at manipulere mellemlagskoblingen af -
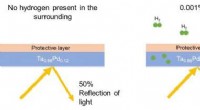 Forskere udvikler en alsidig brintsensorFigur 1. Skematisk illustration af, hvordan optiske brintsensorer fungerer. I nærheden af brint, det tantal- (Ta) og palladium- (Pd)-baserede materiale absorberer hydrogen (H). Jo større mængden af
Forskere udvikler en alsidig brintsensorFigur 1. Skematisk illustration af, hvordan optiske brintsensorer fungerer. I nærheden af brint, det tantal- (Ta) og palladium- (Pd)-baserede materiale absorberer hydrogen (H). Jo større mængden af -
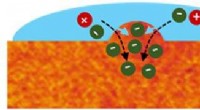 For at forbinde biologi med elektronik, være stiv, alligevel fleksibelEt skematisk billede af P3HT-filmen, viser områder, der er i stand til subtilt at svulme op for at lukke ionmolekyler ind. Kredit:Rajiv Giridharagopal Problemet er en grundlæggende uforenelighed i
For at forbinde biologi med elektronik, være stiv, alligevel fleksibelEt skematisk billede af P3HT-filmen, viser områder, der er i stand til subtilt at svulme op for at lukke ionmolekyler ind. Kredit:Rajiv Giridharagopal Problemet er en grundlæggende uforenelighed i
- Har prokaryoter cellevægge?
- Airbus overskud falder, skyder skylden på skrotning af A380
- Forskere foreslår en ny metode til storskala produktion af termisk stabile enkeltatomkatalysatorer
- Hvad er PCNTR -ledning?
- Hvordan vi løste et arktisk kviksølvmysterium
- Meteorologer siger, at årets varme vinter var nøgleingrediensen til dræber tornadoer fra Midtvest…


