Et emissionsspektrum af et atom produceres, når dets elektroner er.?
Her er en sammenbrud:
* excitation: Når et atom absorberer energi (fra varme, lys eller andre kilder), springer dens elektroner fra deres jordtilstand til højere energiniveau. Dette kaldes excitation.
* de-excitation: De ophidsede elektroner er ustabile og vil vende tilbage til deres lavere energiniveau. For at gøre det frigiver de den absorberede energi i form af lys.
* Emissionsspektrum: Det udsendte lys består af specifikke bølgelængder (farver), der svarer til energiforskellene mellem elektrronens energiniveau. Dette unikke mønster af bølgelængder er atomets emissionsspektrum.
Tænk på det sådan:
* Forestil dig en stige: Gadene på stigen repræsenterer energiniveauet.
* en elektron klatrer op ad stigen: Det absorberer energi og springer til en højere ring.
* elektronet falder tilbage: Det frigiver energi i form af lys, når den falder ned for at sænke trin.
Hvert "trin" ned ad stigen frigiver en bestemt lysfarve og bidrager til atomets unikke emissionsspektrum.
Sidste artikelHvilken til partikler findes i en Atoms -kerne?
Næste artikelHvordan blev elektroner produceret fra katodestrålen?
 Varme artikler
Varme artikler
-
 Højteknologisk sensing belyser betonstresstestEt billede fra et fotonisk kamera, der viser, hvordan brug af belægningen kan skabe en stearinlyslignende flamme, der fremhæver forskydningsspændingsfordelingen i en prøvebetonbjælke. Kredit:Universit
Højteknologisk sensing belyser betonstresstestEt billede fra et fotonisk kamera, der viser, hvordan brug af belægningen kan skabe en stearinlyslignende flamme, der fremhæver forskydningsspændingsfordelingen i en prøvebetonbjælke. Kredit:Universit -
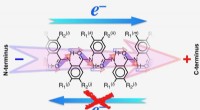 Elektroner tager et skridt fremad uden to skridt tilbageEn bioinspireret molekylær elektretdipol leder alle elektronerne mod den positive pol og forhindrer dem i at bevæge sig mod den negative pol. Kredit:Valentine Vullev Forskere ved University of Cal
Elektroner tager et skridt fremad uden to skridt tilbageEn bioinspireret molekylær elektretdipol leder alle elektronerne mod den positive pol og forhindrer dem i at bevæge sig mod den negative pol. Kredit:Valentine Vullev Forskere ved University of Cal -
 Nyt polymermateriale kan hjælpe batterier med at blive selvhelbredende, genanvendeligtMaterialevidenskab og ingeniørprofessor Christopher Evans, ret, og kandidatstuderende Brian Jing har udviklet en solid batterielektrolyt, der både er selvhelbredende og genanvendelig. Kredit:L. Brian
Nyt polymermateriale kan hjælpe batterier med at blive selvhelbredende, genanvendeligtMaterialevidenskab og ingeniørprofessor Christopher Evans, ret, og kandidatstuderende Brian Jing har udviklet en solid batterielektrolyt, der både er selvhelbredende og genanvendelig. Kredit:L. Brian -
 Regn, regn, gå væk:Ny vandtætningsløsning opdagetKredit:CC0 Public Domain En ny belægningsløsning opdaget af forskere ved Simon Fraser University kan forvandle almindelige materialer til vandtætte overflader. Produktet vil være billigere at prod
Regn, regn, gå væk:Ny vandtætningsløsning opdagetKredit:CC0 Public Domain En ny belægningsløsning opdaget af forskere ved Simon Fraser University kan forvandle almindelige materialer til vandtætte overflader. Produktet vil være billigere at prod
- Hvad sker der med stof og et objekts partikler under fysisk forandring?
- Hvad er Eddy i vejret?
- Hvilke elementer udgør glukose?
- Kernza:Det miljøvenlige hvedeafgrøde, der ønsker at fodre verden
- Undersøgelse kaster lys over, hvordan kulturer adskiller sig i deres tro på lykke
- Hvad måler du masse med i det metriske system?


