Hvad er kovalente hydrider?
kovalente hydrider:Deling af kærlighed til elektroner
Kovalente hydrider er forbindelser dannet, når hydrogenatomer deler elektroner med ikke -metaller. Disse forbindelser er kendetegnet ved tilstedeværelsen af kovalente bindinger mellem brint og ikke -metal.
Her er en oversigt over deres nøglefunktioner:
1. Dannelse:
* kovalent binding: Hydrogen deler elektroner med et ikke -metalatom, hvilket skaber en kovalent binding. Dette sker, fordi elektronegativitetsforskellen mellem brint og ikke -metal er lille, hvilket fører til deling snarere end fuldstændig overførsel af elektroner.
* ikke -metalpartnere: Ikke -metaller inkluderer elementer som bor (B), carbon (C), nitrogen (N), ilt (O), fluor (F), chlor (CL) osv.
2. Egenskaber:
* gasformig eller flygtig: De fleste kovalente hydrider er gasser ved stuetemperatur, hvor nogle er flygtige væsker (som vand).
* lave kogepunkter: På grund af svage intermolekylære kræfter (som van der Waals -styrker) har de relativt lave kogepunkter.
* brændbar: Mange kovalente hydrider er brandfarlige. For eksempel er metan (CH4) den primære komponent i naturgas.
3. Eksempler:
* gruppe 14: Methan (CH4), Silane (SIH4), Germane (GEH4), Stannane (SNH4).
* gruppe 15: Ammoniak (NH3), phosphin (PH3), Arsine (ASH3), Stibine (SBH3).
* gruppe 16: Vand (H2O), hydrogensulfid (H2S), hydrogen selenid (H2SE), hydrogen tellurid (H2TE).
* gruppe 17: Hydrogenfluorid (HF), hydrogenchlorid (HCI), hydrogenbromid (HBR), hydrogeniodid (HI).
4. Betydning:
* Industrielle applikationer: Mange kovalente hydrider har betydelige industrielle anvendelser. For eksempel er metan en primær brændstofkilde, mens ammoniak bruges i gødningsproduktion.
* Grundlæggende kemi: At studere kovalente hydrider hjælper med at forstå arten af kovalente binding og dens indflydelse på molekylære egenskaber.
5. Nøgleforskel fra ioniske hydrider:
* ioniske hydrider: Dannet af reaktionen af brint med alkalimetaller (gruppe 1) eller alkaliske jordmetaller (gruppe 2). I disse forbindelser findes der brint som en hydridion (H-) på grund af overførsel af elektroner.
Husk, at kovalente hydrider er en forskelligartet gruppe af forbindelser, der spiller afgørende roller på forskellige felter. Det er vigtigt at forstå deres egenskaber og egenskaber for at forstå deres betydning i kemi og videre.
 Varme artikler
Varme artikler
-
 Krympefilm får grebKredit:American Chemical Society Mange mennesker husker med glæde at lege med legetøj kendt som Shrinky Dinks - plader af polystyrenplast med former, som børn kan farve, skær ud og varm i en ovn,
Krympefilm får grebKredit:American Chemical Society Mange mennesker husker med glæde at lege med legetøj kendt som Shrinky Dinks - plader af polystyrenplast med former, som børn kan farve, skær ud og varm i en ovn, -
 Titaniumatom, der findes to steder på én gang i krystal, skyld i usædvanligt fænomenDette højopløselige scanningselektronmikroskop (SEM) billede af BaTiS 3 krystaller er overlejret med illustrationer, der viser orienteringen af individuelle atomer i krystallen. På trods af krysta
Titaniumatom, der findes to steder på én gang i krystal, skyld i usædvanligt fænomenDette højopløselige scanningselektronmikroskop (SEM) billede af BaTiS 3 krystaller er overlejret med illustrationer, der viser orienteringen af individuelle atomer i krystallen. På trods af krysta -
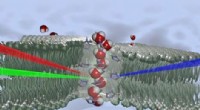 Kunstige bio-inspirerede membraner til vandfiltreringSkematisk repræsentation af vandmolekyler med en trådlignende struktur orienteret i en enkelt retning i kernen af en kanal, vist som gennemsigtig. Dannet af histaminderivater, denne chirale kanal da
Kunstige bio-inspirerede membraner til vandfiltreringSkematisk repræsentation af vandmolekyler med en trådlignende struktur orienteret i en enkelt retning i kernen af en kanal, vist som gennemsigtig. Dannet af histaminderivater, denne chirale kanal da -
 Hvordan elektroderne i lithium-luftbatterier bliver passiveredeEn elektrokemisk celle til studier af processers mekanismer, foregår i lithium-luft-batterier. Kredit:Alexei Khokhlov Lithium-luft-batterier producerer strøm fra luft, og kaldes ofte lithium-oxyge
Hvordan elektroderne i lithium-luftbatterier bliver passiveredeEn elektrokemisk celle til studier af processers mekanismer, foregår i lithium-luft-batterier. Kredit:Alexei Khokhlov Lithium-luft-batterier producerer strøm fra luft, og kaldes ofte lithium-oxyge
- Philips lukker fabrikken i Storbritannien på grund af geopolitiske bekymringer
- Sådan ser du de bedste meteorbyger fra 2010:Værktøjer, tips og 'Gem datoer'
- Verdens første optiske fiberlaser lover at revolutionere detektion af gasser til industrien
- Hvorfor betragtes vi som stjerne ting?
- Sådan testes et NiCad-batteri
- Hvordan molekylære systemer ved livets oprindelse kan have udviklet sig:Nanomaskinernes stigning


