En vandig opløsning, der indeholder et ikke -flygtigt opløst stof, koger over 100 Celsius ved 1 ATM -tryk sand eller falsk?
Her er hvorfor:
* kogepunkthøjde: Når et ikke -flygtigt opløst stof (en, der ikke let fordamper) tilsættes til et opløsningsmiddel (som vand), forstyrrer det opløsningsmidlets damptryk. Solute -molekylerne forstyrrer opløsningsmiddelmolekylerne, der slipper ud i gasfasen.
* Højere damptryk kræves: For at nå kogepunktet (hvor damptrykket er lig med atmosfæretrykket), har opløsningen nu brug for en højere temperatur. Dette skyldes, at tilstedeværelsen af opløsningen har sænket opløsningsmidlets damptryk.
* 1 atm: Ved et standardtryk på 1 atmosfære koges rent vand ved 100 grader Celsius. Imidlertid skal opløsningen nå en temperatur over 100 grader Celsius for at opnå det samme damptryk og kogte.
Fortæl mig, hvis du gerne vil have flere detaljer om kogepunkthøjde!
Sidste artikelHvad er det at sprede affald?
Næste artikelEr Jorden kerne en solid eller væske?
 Varme artikler
Varme artikler
-
 Samarbejde former ekstracellulær vesikelretentionsstrategiKredit:CC0 Public Domain At udnytte unik ekspertise i samarbejdets ånd er en af Carnegie Mellon Universitys formler for succes. I løbet af de sidste tre år har Phil Campbell og Xi (Charlie) Ren s
Samarbejde former ekstracellulær vesikelretentionsstrategiKredit:CC0 Public Domain At udnytte unik ekspertise i samarbejdets ånd er en af Carnegie Mellon Universitys formler for succes. I løbet af de sidste tre år har Phil Campbell og Xi (Charlie) Ren s -
 Maskinlæring opdager nye sekvenser for at booste medicinleveringMIT-forskere kombinerede eksperimentel kemi med kunstig intelligens for at opdage ikke-giftige, højaktive peptider, der kan bindes til phosphorodiamidat morpholino-oligomerer (PMO) for at hjælpe med l
Maskinlæring opdager nye sekvenser for at booste medicinleveringMIT-forskere kombinerede eksperimentel kemi med kunstig intelligens for at opdage ikke-giftige, højaktive peptider, der kan bindes til phosphorodiamidat morpholino-oligomerer (PMO) for at hjælpe med l -
 Ny tekstilfarvningsmetode reducerer drastisk vandbehov og giftig udledning af farvestoffer drastiskAnuradhi Liyanapathiranage er ph.d. kandidat i College of Family and Consumer Sciences. Kredit:Nancy Evelyn/UGA Anuradhi Liyanapathiranage brænder for bæredygtighed og beskyttelse af miljøet genne
Ny tekstilfarvningsmetode reducerer drastisk vandbehov og giftig udledning af farvestoffer drastiskAnuradhi Liyanapathiranage er ph.d. kandidat i College of Family and Consumer Sciences. Kredit:Nancy Evelyn/UGA Anuradhi Liyanapathiranage brænder for bæredygtighed og beskyttelse af miljøet genne -
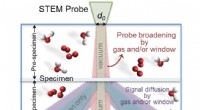 Bestemmelse af parametrene for transmissionselektronmikroskopiGaseffekter på spredning af hurtige elektroner, der bidrager til ESTEM -sonden og signalet. Kredit:Pacific Northwest National Laboratory Selvom telefonerne i vores lommer måske er perfekte til at
Bestemmelse af parametrene for transmissionselektronmikroskopiGaseffekter på spredning af hurtige elektroner, der bidrager til ESTEM -sonden og signalet. Kredit:Pacific Northwest National Laboratory Selvom telefonerne i vores lommer måske er perfekte til at
- Hvilket ikke spiller en rolle i at nære det udviklende embryo og foster?
- Topologisk isolator metamateriale med kæmpe cirkulær fotogalvanisk effekt
- Nye isolatorer med ledende kanter
- Forskning i orme giver en model til at studere, hvordan mikrobiomet påvirker sygdomsmennesker
- Hvor meget porøsitet holder ler?
- Defekte nanorør blev til lysgivere


