Hvorfor er dipolinteraktioner svage?
* Afstandsafhængighed: Styrken af dipol-dipolinteraktioner falder hurtigt med afstand. Dette skyldes, at tiltrækningskraften mellem de positive og negative ender af dipolerne svækkes, når afstanden mellem dem øges. Dette gør dem meget svagere end ioniske eller kovalente bindinger, som har meget stærkere kræfter.
* Orienteringsafhængighed: Dipol-dipolinteraktioner er også meget afhængige af orienteringen af molekylerne. De stærkeste interaktioner forekommer, når den positive ende af et molekyle er på linje med den negative ende af en anden. Imidlertid forstyrrer termisk bevægelse konstant disse justeringer og svækker i gennemsnit interaktionen.
* Størrelse af dipolmoment: Styrken af interaktionen er også direkte proportional med størrelsen af molekylets dipolmoment. Molekyler med større dipolmomenter vil have stærkere interaktioner. Selv med store dipolmomenter er interaktionerne dog stadig relativt svage sammenlignet med andre typer intermolekylære kræfter.
Sammenligning med andre interaktioner:
* kovalente obligationer: Disse involverer deling af elektroner og er signifikant stærkere end dipol-dipol-interaktioner.
* ioniske bindinger: Disse involverer den elektrostatiske tiltrækning mellem ioner og er også meget stærkere end dipol-dipol-interaktioner.
* Hydrogenbindinger: Mens de stadig er svagere end kovalente og ioniske bindinger, er brintbindinger stærkere end dipol-dipolinteraktioner på grund af den stærke elektronegativitetsforskel mellem brint og det andet involverede atom.
Kortfattet:
* Dipol-dipolinteraktioner er svage, fordi de er afhængige af svagere elektrostatiske kræfter sammenlignet med kovalente eller ioniske bindinger.
* Interaktionerne er følsomme over for afstand og orientering, hvilket gør dem endnu svagere på grund af termisk bevægelse.
* Størrelsen af dipolmomentet påvirker styrken, men selv med store dipoler forbliver interaktionerne relativt svage.
Det er vigtigt at huske, at selvom svage, dipol-dipol-interaktioner stadig er vigtige i mange kemiske og biologiske processer. De bidrager til egenskaberne ved væsker, påvirker smeltnings- og kogepunkterne for molekyler og spiller en rolle i proteinfoldning og molekylær genkendelse.
Sidste artikelHvor mange atomer kan passe i 1 skal?
Næste artikelHvorfor er den ydre kerne væske, men indre fast stof?
 Varme artikler
Varme artikler
-
 En opgradering til magnetiske resonansmetoder med en 1.000-fold forstærkerKredit:CC0 Public Domain Forskere bestemmer strukturen og dynamikken af proteiner ved hjælp af NMR (Nuclear Magnetic Resonance) spektroskopi. Indtil nu har det dog været nødvendigt med meget høje
En opgradering til magnetiske resonansmetoder med en 1.000-fold forstærkerKredit:CC0 Public Domain Forskere bestemmer strukturen og dynamikken af proteiner ved hjælp af NMR (Nuclear Magnetic Resonance) spektroskopi. Indtil nu har det dog været nødvendigt med meget høje -
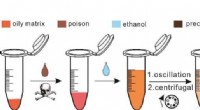 Ethanol-ekstraktion SERS-strategi giver meget følsom påvisning af giftstoffer i olieagtig matrixSkematisk diagram af SERS-detektion baseret på ethanolekstraktion. Kredit:WANG Yongtao Forskere fra det kinesiske videnskabsakademi (CAS) udviklede for nylig en ethanol-ekstraktionsoverfladeforstæ
Ethanol-ekstraktion SERS-strategi giver meget følsom påvisning af giftstoffer i olieagtig matrixSkematisk diagram af SERS-detektion baseret på ethanolekstraktion. Kredit:WANG Yongtao Forskere fra det kinesiske videnskabsakademi (CAS) udviklede for nylig en ethanol-ekstraktionsoverfladeforstæ -
 Undersøgelse afslører korrosionsmekanisme af magnesiumlegeringer i marine atmosfærisk miljøDe optiske fotografier af mikrostruktur for Mg-5Y-1.5Nd-xZn-0.5Zr (x = 0, 2, 4, 6 wt.%) legeringer. Kredit:Journal of Magnesium and Alloys (2022). DOI:10.1016/j.jma.2022.03.007 Magnesiumlegeringer
Undersøgelse afslører korrosionsmekanisme af magnesiumlegeringer i marine atmosfærisk miljøDe optiske fotografier af mikrostruktur for Mg-5Y-1.5Nd-xZn-0.5Zr (x = 0, 2, 4, 6 wt.%) legeringer. Kredit:Journal of Magnesium and Alloys (2022). DOI:10.1016/j.jma.2022.03.007 Magnesiumlegeringer -
 Nyt twist i løbet om at udskifte grafitanoden til bedre genopladelige batterierKredit:UC San Diego Jacobs School of Engineering Forbedringer af en klasse af batterielektrolyt, der først blev introduceret i 2017-flydende gaselektrolytter-kunne bane vejen til et kraftigt og læ
Nyt twist i løbet om at udskifte grafitanoden til bedre genopladelige batterierKredit:UC San Diego Jacobs School of Engineering Forbedringer af en klasse af batterielektrolyt, der først blev introduceret i 2017-flydende gaselektrolytter-kunne bane vejen til et kraftigt og læ
- Strøm af materiale observeret for første gang omkring en ung eruptiv stjerne
- Undersøgelse tyder på optimale sociale netværk på ikke mere end 150 personer
- Hvilke em -bølger udsendes af ild?
- Hvordan konserverer og genopretter vi computerbaseret kunst i et foranderligt teknologisk miljø?
- Hvornår skal gul sten -super vulkan udbryde?
- Hvad er vigtigheden af fossiler?


