Hvad er forskellen mellem kemiske og fysiske ændringer?
Fysiske ændringer:
* Ingen nye stoffer dannes. Molekylerne i sig selv forbliver de samme, men deres arrangement eller stofstilstand kan ændre sig.
* ofte reversibel. Det originale stof kan gendannes på enkle midler.
* involverer normalt ændringer i fysiske egenskaber som form, størrelse, farve, tilstand af stof (fast, flydende, gas), densitet osv.
Eksempler:
* Meltis: Vand skifter fra fast til væske, men dets kemiske sammensætning (H₂O) forbliver den samme.
* kogende vand: Vand skifter fra væske til gas, men det er stadig vand.
* Skærepapir: Papiret ændrer form, men dens kemiske makeup forbliver den samme.
* opløste sukker i vand: Sukkeret forsvinder, men det er stadig til stede i vandet som opløste sukkermolekyler.
Kemiske ændringer:
* nye stoffer dannes. Atomerne omarrangeres for at danne nye molekyler med forskellige egenskaber.
* normalt irreversibel. De originale stoffer kan ikke let gendannes.
* involverer ofte ændringer i kemiske egenskaber som brandbarhed, reaktivitet og surhedsgrad.
Eksempler:
* brændende træ: Træ reagerer med ilt for at producere aske, kuldioxid og vand - helt forskellige stoffer.
* rustende jern: Jern reagerer med ilt og vand for at danne jernoxid (rust), et andet stof.
* bagning af en kage: Ingredienserne reagerer med hinanden for at danne en kage, et nyt stof med forskellige egenskaber.
* fordøjelse af mad: Maden er opdelt i enklere molekyler og skaber helt forskellige stoffer.
Her er en enkel måde at huske forskellen på:
* Fysiske ændringer: Du kan normalt vende ændringen og få det originale stof tilbage. Tænk på det som at ændre udseendet men ikke den grundlæggende sammensætning.
* Kemiske ændringer: Du kan normalt ikke vende ændringen let. Tænk på det som at skabe noget helt nyt med forskellige egenskaber.
Sidste artikelHvad er den estimerede atomvægt af radium?
Næste artikelKan en kemisk ændring vendes ved forandring?
 Varme artikler
Varme artikler
-
 En højtydende nanopulverfacilitet til 3-D-tryk i metalKredit:Tomsk Polytechnic University (TPU) Forskere fra afdelingen for industrielle teknologier ved Yurga Institute of Technology ved Tomsk Polytechnic University udvikler en avanceret højtydende f
En højtydende nanopulverfacilitet til 3-D-tryk i metalKredit:Tomsk Polytechnic University (TPU) Forskere fra afdelingen for industrielle teknologier ved Yurga Institute of Technology ved Tomsk Polytechnic University udvikler en avanceret højtydende f -
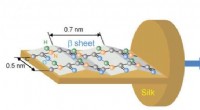 Ny infrarød billeddannelsesteknik afslører molekylær orientering af proteiner i silkefibreOrienteringen af C =O, C-N, og NH-bindinger i amidstruktur af L-sektionen af silkefibre bekræftet i denne undersøgelse af hyper-spektral billeddannelse. Kredit:Australian Synchrotron Et stort
Ny infrarød billeddannelsesteknik afslører molekylær orientering af proteiner i silkefibreOrienteringen af C =O, C-N, og NH-bindinger i amidstruktur af L-sektionen af silkefibre bekræftet i denne undersøgelse af hyper-spektral billeddannelse. Kredit:Australian Synchrotron Et stort -
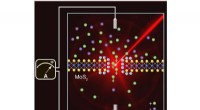 Produktion af elektricitet ved flodmundinger ved hjælp af lys og osmoseGengivelse af de forhold, der opstår ved flodmundinger, EPFL -forskere skinnede lys på et system, der kombinerer vand, salt og en membran på kun tre atomer tykke for at generere mere elektricitet. Kre
Produktion af elektricitet ved flodmundinger ved hjælp af lys og osmoseGengivelse af de forhold, der opstår ved flodmundinger, EPFL -forskere skinnede lys på et system, der kombinerer vand, salt og en membran på kun tre atomer tykke for at generere mere elektricitet. Kre -
 Nyt ledende polymerblæk åbner for næste generation af trykt elektronikForskere ved Linköpings Universitet, Sverige, har udviklet et stabilt polymerblæk med høj ledningsevne. Det nye n-type materiale kommer i form af blæk med ethanol som opløsningsmiddel. Kredit:Thor Bal
Nyt ledende polymerblæk åbner for næste generation af trykt elektronikForskere ved Linköpings Universitet, Sverige, har udviklet et stabilt polymerblæk med høj ledningsevne. Det nye n-type materiale kommer i form af blæk med ethanol som opløsningsmiddel. Kredit:Thor Bal
- Hvilke atomer findes i alle makromolekyler?
- Har LHC fundet nogen praktisk anvendelse til Higgs boson?
- SoftBank rapporterer skyhøjt årligt driftsresultat
- Selvdrevne fleksible flerfarvede elektrokrome enheder til informationsdisplays
- Hvordan man opbygger en ovn til et videnskabsprojekt
- Hvorfor er rovdyret øverst på fødevarekæden mest risiko for bioakkumulering?


