Opløs salt hurtigere i vandet end sukker?
* Polaritet: Sukkermolekyler (saccharose) er mere polære end saltmolekyler (natriumchlorid). Dette betyder, at de har en stærkere tiltrækning til vandmolekyler, som også er polære. Den stærkere attraktion fører til hurtigere opløsning.
* krystalstruktur: Saltkrystaller har en tæt pakket, kubisk struktur, hvilket gør det sværere for vandmolekyler at trænge igennem og bryde krystallen fra hinanden. Sukkerkrystaller har en løsere, mere åben struktur, hvilket muliggør lettere interaktion med vandmolekyler.
* Temperatur: Både salt og sukker opløses hurtigere ved højere temperaturer. Dette skyldes, at den øgede kinetiske energi af vandmolekylerne gør det lettere at bryde de opløste molekyler fra hinanden.
Der er dog faktorer, der kan påvirke opløsningshastigheden for begge stoffer:
* omrøring: Omrøring eller agitation hjælper med at bringe friske vandmolekyler i kontakt med opløsningen, hvilket øger opløsningshastigheden for både salt og sukker.
* Partikelstørrelse: Mindre partikler af salt og sukker opløses hurtigere end større partikler. Dette skyldes, at der er mere overfladeareal udsat for vandet.
* Koncentration: Når koncentrationen af salt eller sukker i vandet øges, bremser opløsningshastigheden. Dette skyldes, at vandet bliver mættet med opløsningen.
Konklusion: Mens sukker generelt opløses hurtigere end salt i vand, kan forskellige faktorer påvirke opløsningshastigheden for begge stoffer.
Sidste artikelHvorfor lave et efterforskningsprojekt af frugtbatterier?
Næste artikelHvilke ting er lavet med videnskab?
 Varme artikler
Varme artikler
-
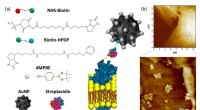 En biosensor til måling af ekstracellulære hydrogenperoxidkoncentrationerFigur 1:(a) Forklarende skitse af plasmamembranen forankret nanosensor. De forbindelser, der bruges til guldnanopartikler (AuNP) -konjugering, er den H2O2-følsomme 4-mercaptophenylboroniske pinacolest
En biosensor til måling af ekstracellulære hydrogenperoxidkoncentrationerFigur 1:(a) Forklarende skitse af plasmamembranen forankret nanosensor. De forbindelser, der bruges til guldnanopartikler (AuNP) -konjugering, er den H2O2-følsomme 4-mercaptophenylboroniske pinacolest -
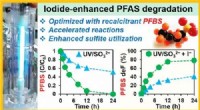 PFAS-kemikalier holder ikke evigtGrafisk abstrakt. Kredit:Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c07608 Når de først er blevet kaldt kemikalier for evigt, kan per- og polyfluoralkyl-stoffer eller PFAS være
PFAS-kemikalier holder ikke evigtGrafisk abstrakt. Kredit:Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c07608 Når de først er blevet kaldt kemikalier for evigt, kan per- og polyfluoralkyl-stoffer eller PFAS være -
 Forskning afslører, hvorfor det er svært at få lugten ud af polyesterKredit:Unsplash/CC0 Public Domain Hvorfor er den yndlingsskjorte den du har båret rundt i huset siden COVID-19 startede, stadig stinker, selv efter almindelig vask? Sandsynligvis indeholder det p
Forskning afslører, hvorfor det er svært at få lugten ud af polyesterKredit:Unsplash/CC0 Public Domain Hvorfor er den yndlingsskjorte den du har båret rundt i huset siden COVID-19 startede, stadig stinker, selv efter almindelig vask? Sandsynligvis indeholder det p -
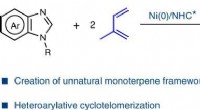 Forskere indser nikkel-katalyseret asymmetrisk heteroarylativ cyclotelomerisering af isoprenGrafisk abstrakt. Kredit:Nature Catalysis (2022). DOI:10.1038/s41929-022-00825-z Isopren bruges som en forløber til at producere terpener og terpenoider. Den direkte katalytiske omdannelse af isopr
Forskere indser nikkel-katalyseret asymmetrisk heteroarylativ cyclotelomerisering af isoprenGrafisk abstrakt. Kredit:Nature Catalysis (2022). DOI:10.1038/s41929-022-00825-z Isopren bruges som en forløber til at producere terpener og terpenoider. Den direkte katalytiske omdannelse af isopr


