Hvorfor tror du, at polære og ikke -polære molekyler ikke blandes?
polære molekyler:
* ujævn fordeling af ladning: Polære molekyler har en positiv og negativ ende på grund af forskelle i elektronegativitet mellem deres atomer. Dette skaber et dipolmoment .
* stærkere intermolekylære kræfter: Polære molekyler tiltrækker hinanden gennem dipol-dipol-interaktioner og hydrogenbinding (Hvis de indeholder hydrogen bundet til ilt, nitrogen eller fluor). Disse kræfter er relativt stærke.
ikke -polære molekyler:
* Even Distribution of Charge: Ikke -polære molekyler har en jævn fordeling af ladning. De har ikke et permanent dipolmoment.
* svagere intermolekylære kræfter: Ikke -polære molekyler interagerer kun gennem London Dispersion Forces , som er meget svage.
hvorfor de ikke blander:
* opløselighed: "Som opløser som" er en generel regel inden for kemi. Polære molekyler har en tendens til at opløses i polære opløsningsmidler (f.eks. Vand), mens ikke -polære molekyler opløses i ikke -polære opløsningsmidler (f.eks. Olie).
* Intermolekylær Force Mismatch: Når polære og ikke -polære molekyler samles, kan de ikke danne stærke intermolekylære bindinger med hinanden. De svage interaktioner mellem dem er ikke nok til at overvinde de stærkere kræfter inden for hver type molekyle.
* adskillelse: Som et resultat vil de polære molekyler klæbe sammen og danne deres egen fase (f.eks. Vanddråber), mens de ikke -polære molekyler danner en anden fase (f.eks. Olielag). Dette fører til ublandbarhed (manglende evne til at blande).
Eksempel: Olie og vand er et klassisk eksempel. Olie er et ikke -polært stof, mens vand er polært. Når du blander dem, danner vandmolekylerne brintbindinger med hinanden, eksklusive oliemolekylerne. Dette skaber to forskellige lag.
Kortfattet: Forskellene i intermolekylære kræfter mellem polære og ikke -polære molekyler er den primære årsag til deres inkompatibilitet og mangel på blanding.
Sidste artikelHvad er enorme kugler af gasser?
Næste artikelHvis koldt vand er isvand, hvilket blæk?
 Varme artikler
Varme artikler
-
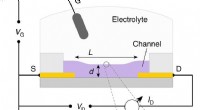 Ny metode benchmarks organiske blandede ledereOECT beskrivelse og betjening. et OECT -tværsnit, ledninger, og dimensioner:kanallængde (L), og tykkelse (d). Kilden, dræne, og port (S, D, G, henholdsvis), og relevante spændinger (gate, afløbsspændi
Ny metode benchmarks organiske blandede ledereOECT beskrivelse og betjening. et OECT -tværsnit, ledninger, og dimensioner:kanallængde (L), og tykkelse (d). Kilden, dræne, og port (S, D, G, henholdsvis), og relevante spændinger (gate, afløbsspændi -
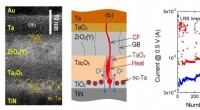 En optimeret struktur af memristiv enhed til neuromorfe computersystemerHøjopløselig transmissionselektronmikroskopibillede (a) og skematisk (b) af tværsnittet af flerlags memristive strukturen i området for den ledende filament (CF), afhængigheden af resistive tilstand
En optimeret struktur af memristiv enhed til neuromorfe computersystemerHøjopløselig transmissionselektronmikroskopibillede (a) og skematisk (b) af tværsnittet af flerlags memristive strukturen i området for den ledende filament (CF), afhængigheden af resistive tilstand -
 Forståelse og styring af det molekyle, der skabte universetMarcos Dantus, Universitets fremtrædende professor i kemi og fysik, har genskabt interstellare ioner med lasere. Kredit:MSU Trihydrogen, eller H 3 + , er anerkendt af videnskabsmænd som det mo
Forståelse og styring af det molekyle, der skabte universetMarcos Dantus, Universitets fremtrædende professor i kemi og fysik, har genskabt interstellare ioner med lasere. Kredit:MSU Trihydrogen, eller H 3 + , er anerkendt af videnskabsmænd som det mo -
 Gennemgang af den seneste udvikling inden for elektrolyse af saltvandKredit:CC0 Public Domain Solcelledrevet teknologi, såsom fotovoltaik (PVer), kunne løse nogle af vores tids miljøudfordringer, muliggør bæredygtig produktion af elektrisk energi i mange geografisk
Gennemgang af den seneste udvikling inden for elektrolyse af saltvandKredit:CC0 Public Domain Solcelledrevet teknologi, såsom fotovoltaik (PVer), kunne løse nogle af vores tids miljøudfordringer, muliggør bæredygtig produktion af elektrisk energi i mange geografisk
- Et gennembrud inden for forskning i chiral polymer tyndfilm kunne muliggøre en ny generation af enh…
- Hvad er 225 Fahrenheit lig i Celsius?
- Forskere kortlægger Mars globale vindmønstre for første gang
- Walmart one-ups Amazon med leveringer direkte til køleskabet
- Hvordan planter udviklede sig til at klare kulden
- Hvad er de vigtigste landformer og kroppe af vandkuba?


