Når ikke ioniske forbindelser udfører elektricitet?
* solid tilstand: I deres faste tilstand danner ioniske forbindelser en stiv gitterstruktur. Ionerne holdes tæt på plads af stærke elektrostatiske kræfter. Dette faste arrangement forhindrer den frie bevægelse af ioner, hvilket er nødvendigt for elektrisk ledningsevne.
* vandig løsning: Når en ionisk forbindelse opløses i vand, omgiver vandmolekylerne ionerne og trækker dem fra hinanden og bryder gitterstrukturen. Disse frie ioner er nu i stand til at bevæge sig gennem opløsningen og bære en elektrisk strøm.
* smeltet tilstand: Når en ionisk forbindelse opvarmes til dens smeltepunkt, svækkes de stærke elektrostatiske kræfter, der holder ionerne sammen, så ionerne kan bevæge sig frit. Denne frie bevægelse af ioner muliggør den smeltede forbindelse til at udføre elektricitet.
Sammenfattende udfører ioniske forbindelser kun elektricitet, når deres ioner er fri til at bevæge sig. Dette forekommer i vandige løsninger og smeltede tilstande.
 Varme artikler
Varme artikler
-
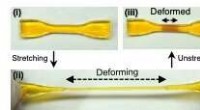 Selvvoksende materialer, der styrker som reaktion på kraftEn dobbeltnetværkshydrogel (i). Efter strækning (ii), skøre sektioner går i stykker, tillader en generation af mekanoradikale stoffer, angivet ved farveændring (iii). Kredit:Gong J.P. et al., Mekanore
Selvvoksende materialer, der styrker som reaktion på kraftEn dobbeltnetværkshydrogel (i). Efter strækning (ii), skøre sektioner går i stykker, tillader en generation af mekanoradikale stoffer, angivet ved farveændring (iii). Kredit:Gong J.P. et al., Mekanore -
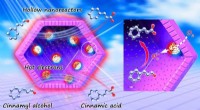 Konstruktion af hule nanoreaktorer til forbedrede fotooxidationerSkematisk diagram af hule nanoreaktorer til fotokatalytisk oxidation af cinnamylalkohol. Kredit:Science China Press Oxidation af primære alkoholer til carboxylsyrer er af betydning i både organisk
Konstruktion af hule nanoreaktorer til forbedrede fotooxidationerSkematisk diagram af hule nanoreaktorer til fotokatalytisk oxidation af cinnamylalkohol. Kredit:Science China Press Oxidation af primære alkoholer til carboxylsyrer er af betydning i både organisk -
 Forskere identificerer enzym, der er ansvarligt for at hjælpe kræfttumorer med at sprede sigSteven Van Doren afslørede, hvordan et kræftkritisk enzym er placeret på celleoverflader. Kredit:University of Missouri-Columbia Forskere ved University of Missouri har opdaget, hvordan et kræftkr
Forskere identificerer enzym, der er ansvarligt for at hjælpe kræfttumorer med at sprede sigSteven Van Doren afslørede, hvordan et kræftkritisk enzym er placeret på celleoverflader. Kredit:University of Missouri-Columbia Forskere ved University of Missouri har opdaget, hvordan et kræftkr -
 Farvelægning af hjerteslagHjertesygdomme er en af de førende dødsårsager rundt om i verden. At finde lette tidlige måder at screene efter gode lægemidler er afgørende. Kredit:Kyoto University iCeMS I det 17. århundrede t
Farvelægning af hjerteslagHjertesygdomme er en af de førende dødsårsager rundt om i verden. At finde lette tidlige måder at screene efter gode lægemidler er afgørende. Kredit:Kyoto University iCeMS I det 17. århundrede t


