Hvorfor uranbrændstof bliver til oxid?
* stabilitet: Urandioxid er en meget stabil forbindelse, hvilket gør det velegnet til atomreaktorer. Det er relativt modstandsdygtigt over for kemisk angreb og opløses ikke let i vand.
* smeltepunkt: UO2 har et højt smeltepunkt, hvilket betyder, at det kan modstå de høje temperaturer, der genereres i reaktorkernen.
* neutronabsorption: UO2 har en lavere neutronabsorptionshastighed sammenlignet med andre uranforbindelser, hvilket muliggør effektive fissionsreaktioner.
* brændstoffremstilling: UO2 fremstilles let i pellets, den form, hvori den bruges i brændstofstænger.
Under drift i en atomreaktor kan nogle urandioxid imidlertid oxideres yderligere for at danne urantrioxid (UO3) og andre oxider:
* Høje temperaturer: Den ekstreme varme inde i reaktorkernen kan forårsage en vis oxidation.
* ilt tilstedeværelse: Der er en lille mængde ilt til stede i reaktorens kølevæske, som kan bidrage til oxidation.
* Bestrålingsskade: Det intense strålingsmiljø inden for reaktoren kan forårsage strukturelle ændringer i UO2 -gitteret, hvilket gør det mere modtageligt for oxidation.
Denne yderligere oxidation er typisk en mindre effekt og styres gennem reaktordesign og -drift. Den primære form for uran i brændstoffet forbliver UO2, men en eller anden oxidation forventes og redegøres for.
Sidste artikelHvad er 2 molekyler, der indeholder uran?
Næste artikelHvilke elementer kan uran kombineres med for at danne en forbindelse?
 Varme artikler
Varme artikler
-
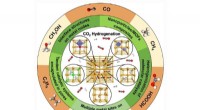 Gennemgang af teknologier, der øger potentialet for kuldioxidkonvertering til nyttige produkterMed de veldefinerede retikulære rammer og fleksible modificerbarhed kan metal-organiske rammer (MOFer) være den ideelle platform til at konstruere de aktiverede katalysatorer til carbondioxidhydrogene
Gennemgang af teknologier, der øger potentialet for kuldioxidkonvertering til nyttige produkterMed de veldefinerede retikulære rammer og fleksible modificerbarhed kan metal-organiske rammer (MOFer) være den ideelle platform til at konstruere de aktiverede katalysatorer til carbondioxidhydrogene -
 Foring af MOF-lommer til at detektere skadelige gasserSvovldioxidmolekyler (røde og gule) optages selektivt af porer i den metalorganiske struktur. Kredit:Valeriya Chernikova Et porøst materiale med skræddersyede lommer syet ind i dets struktur er et
Foring af MOF-lommer til at detektere skadelige gasserSvovldioxidmolekyler (røde og gule) optages selektivt af porer i den metalorganiske struktur. Kredit:Valeriya Chernikova Et porøst materiale med skræddersyede lommer syet ind i dets struktur er et -
 Forskere opfinder ny katalysator til omdannelse af kuldioxidDr Edwin S. Gnanakumar driver den katalytiske strøm. Kredit:HIMS/UvA Forskere fra University of Amsterdam (UvA) har opfundet en ny katalysator, der effektivt kan omdanne kuldioxid (CO2) til kulilt
Forskere opfinder ny katalysator til omdannelse af kuldioxidDr Edwin S. Gnanakumar driver den katalytiske strøm. Kredit:HIMS/UvA Forskere fra University of Amsterdam (UvA) har opfundet en ny katalysator, der effektivt kan omdanne kuldioxid (CO2) til kulilt -
 Escherichia coli-bakterier kaprer kobber, fodre af detEscherichia coli ( E coli ) bakterier (gule) inficerer en museblære. En immuncelle er vist med blåt. En ny undersøgelse fra Washington University School of Medicine i St. Louis viser, hvordan E. co
Escherichia coli-bakterier kaprer kobber, fodre af detEscherichia coli ( E coli ) bakterier (gule) inficerer en museblære. En immuncelle er vist med blåt. En ny undersøgelse fra Washington University School of Medicine i St. Louis viser, hvordan E. co


