Hvad er den mest stabile ion for antimonatom?
Her er hvorfor:
* Elektronkonfiguration: Antimon har en elektronkonfiguration af [KR] 4D 10 5s 2 5p 3 .
* tendens til at miste elektroner: Antimon har en tendens til at miste elektroner for at opnå en stabil ædelgaskonfiguration.
* Valenselektroner: Antimon har 5 valenselektroner (dem i den yderste skal).
* stabilitet: At miste 3 elektroner resulterer i en SB 3+ ion med den stabile konfiguration af [KR] 4D 10 , som er isoelektronisk med den ædle gas krypton.
Mens SB 5+ er også en mulig ion, den er mindre stabil end SB 3+ Fordi det kræver fjernelse af alle fem valenselektroner, hvilket er mere energisk krævende.
 Varme artikler
Varme artikler
-
 Forbedring af ydeevnen af metal-organiske rammematerialerMikrograffoto (samlet bredde ca. 1, 5 mm), der viser det nye adsorberende materiale, der blev fremstillet ved anvendelse af et poppelblad som skabelon. Kanalarkitekturen er tydeligt mærkbar. Tegninger
Forbedring af ydeevnen af metal-organiske rammematerialerMikrograffoto (samlet bredde ca. 1, 5 mm), der viser det nye adsorberende materiale, der blev fremstillet ved anvendelse af et poppelblad som skabelon. Kanalarkitekturen er tydeligt mærkbar. Tegninger -
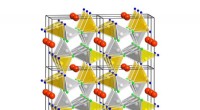 En ny energibesparende LED-fosforKrystalstrukturen af SALON-fosforen er årsagen til dens fremragende luminescensegenskaber. Kredit:University of Innsbruck Det menneskelige øje er særligt følsomt over for grønt, men mindre følso
En ny energibesparende LED-fosforKrystalstrukturen af SALON-fosforen er årsagen til dens fremragende luminescensegenskaber. Kredit:University of Innsbruck Det menneskelige øje er særligt følsomt over for grønt, men mindre følso -
 Fem mærkelige og vidunderlige måder naturen bliver udnyttet til at opbygge en bæredygtig modeindu…Enzymatiske tekstilfarvestoffer. Forfatter oplyst En af de største udfordringer for tekstil- og modeindustrien er at gøre sig selv mere bæredygtig, ikke kun hvad angår økonomiske og arbejdsmæssige
Fem mærkelige og vidunderlige måder naturen bliver udnyttet til at opbygge en bæredygtig modeindu…Enzymatiske tekstilfarvestoffer. Forfatter oplyst En af de største udfordringer for tekstil- og modeindustrien er at gøre sig selv mere bæredygtig, ikke kun hvad angår økonomiske og arbejdsmæssige -
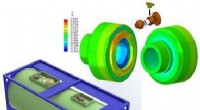 Matematisk model af termoplastisk komposit hjælper med at designe og certificere meget pålidelige …Kredit:Skolkovo Institut for Videnskab og Teknologi Forskere ved Skoltech Center for Design, Manufacturing and Materials og deres kolleger har udviklet og eksperimentelt verificeret modellen af
Matematisk model af termoplastisk komposit hjælper med at designe og certificere meget pålidelige …Kredit:Skolkovo Institut for Videnskab og Teknologi Forskere ved Skoltech Center for Design, Manufacturing and Materials og deres kolleger har udviklet og eksperimentelt verificeret modellen af
- Hvad er almindeligt mellem 1 mol AG og AU?
- Bedre lasere til optisk kommunikation
- Hvordan kan du øge accelerationen med henvisning til masse og kraft?
- Hvad ville din hypotese være med hensyn til, hvordan pH -farven på vand vil ændre sig, når du ud…
- Hvordan man laver en model kvælstof Atom
- Hvor mange forbindelser har den kemiske formel C6H14?


