Hvad er trykket på 4 mol helium i en 50 L tank ved 308 K?
1. Den ideelle gaslov
Den ideelle gaslov er en grundlæggende ligning inden for kemi, der beskriver opførelsen af ideelle gasser. Det udtrykkes som:
PV =NRT
Hvor:
* p er presset fra gassen (i atmosfærer, ATM)
* v er volumen af gassen (i liter, L)
* n er antallet af mol gas
* r er den ideelle gaskonstant (0,0821 l · atm/mol · k)
* t er temperaturen på gassen (i Kelvin, K)
2. Løsning for tryk
Vi ønsker at finde presset (P), så vi kan omarrangere ligningen:
P =(nrt) / v
3. Tilslutning af værdierne
* n =4 mol
* R =0,0821 l · atm/mol · k
* T =308 k
* V =50 l
4. Beregning af trykket
P =(4 mol * 0,0821 L · ATM / mol · K * 308 K) / 50 L
P ≈ 2.03 atm
Derfor er trykket på 4 mol helium i en 50 L tank ved 308 K ca. 2,03 atmosfærer.
 Varme artikler
Varme artikler
-
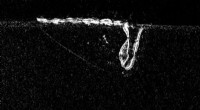 Sprængning af dine (små) bobler:ny forskning peger på vejen mod porefri 3D-printDette røntgenbillede taget ved APS viser en lasersmeltende aluminium under den additive fremstillingsproces. Til venstre for laseren kan du se små porer skabt under processen, som over tid kan skabe f
Sprængning af dine (små) bobler:ny forskning peger på vejen mod porefri 3D-printDette røntgenbillede taget ved APS viser en lasersmeltende aluminium under den additive fremstillingsproces. Til venstre for laseren kan du se små porer skabt under processen, som over tid kan skabe f -
 Forbrændingsadfærd af aromater kan være nøglen til at forbedre udvindingen af tung olieAbstrakt resumé. Kredit:Kazan Federal University Problemet med olieudtømning bliver mere og mere relevant hver dag. Efterhånden som der opstår underskud, ikke-traditionelle og tunge olier, herunde
Forbrændingsadfærd af aromater kan være nøglen til at forbedre udvindingen af tung olieAbstrakt resumé. Kredit:Kazan Federal University Problemet med olieudtømning bliver mere og mere relevant hver dag. Efterhånden som der opstår underskud, ikke-traditionelle og tunge olier, herunde -
 Vandopdeling til konvertering af solenergiPt-modificerede BaTaO2N fotokatalysatorer. Kredit:Citeret fra Wang, Z., Luo, Y., Hisatomi, T. et al. Sekventiel cokatalysatordekoration på BaTaO2N mod højaktiv Z-skema vandspaltning. Nat Commun 12, 10
Vandopdeling til konvertering af solenergiPt-modificerede BaTaO2N fotokatalysatorer. Kredit:Citeret fra Wang, Z., Luo, Y., Hisatomi, T. et al. Sekventiel cokatalysatordekoration på BaTaO2N mod højaktiv Z-skema vandspaltning. Nat Commun 12, 10 -
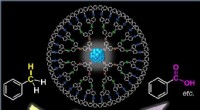 Metalliske nanopartikler lyser op en anden vej mod miljøvenlige katalysatorerHvert dendrimer-molekyle er vært for en metallisk partikel i subnano-størrelse, der muliggør oxidation af aromatiske kulbrinter, såsom toluen (venstre), at producere nyttige organiske forbindelser, så
Metalliske nanopartikler lyser op en anden vej mod miljøvenlige katalysatorerHvert dendrimer-molekyle er vært for en metallisk partikel i subnano-størrelse, der muliggør oxidation af aromatiske kulbrinter, såsom toluen (venstre), at producere nyttige organiske forbindelser, så
- Kovalent Vs. Hydrogen Bonds
- Hvor store er de fleste humane celler?
- Hvad er de fysiske egenskaber og kemiske stoffer skal mønter have?
- Hvilken slags klippe dannes ved forvitring og erosion?
- ATLAS-eksperiment studerer fotonmærket jet-quenching i kvark-gluon-plasmaet
- Amazonskov kan trænes af større nedbørsmængder


