Er Cobalt 3 bromid et solidt?
Her er hvorfor:
* ionisk forbindelse: Cobalt (III) bromid er en ionisk forbindelse, dannet af den elektrostatiske tiltrækning mellem den positivt ladede kobolt (III) ion (co³⁺) og de negativt ladede bromidioner (Br⁻).
* stærke ioniske bindinger: De ioniske bindinger mellem disse ioner er meget stærke, hvilket fører til en stiv, krystallinsk struktur.
* højt smeltepunkt: Ioniske forbindelser har generelt høje smeltepunkter, fordi der kræves en masse energi for at bryde de stærke elektrostatiske kræfter, der holder ionerne sammen.
Derfor eksisterer kobolt (III) bromid som et fast stof ved stuetemperatur på grund af de stærke ioniske bindinger inden for dens struktur.
Sidste artikelHvad er produkterne fra C6H12O6 plus O2?
Næste artikelHvordan adskiller heterogen blanding sig fra et rent stof?
 Varme artikler
Varme artikler
-
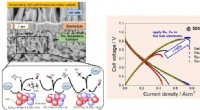 Forskere udvikler højtydende keramisk brændselscelle, der fungerer på butangasNår nikkelkatalysatoren i keramiske brændselsceller bruges sammen med kulbrintebrændstoffer, såsom metan, propan, og butan, det kulstof, der dannes under brændstofomdannelsen, aflejres på overfladen a
Forskere udvikler højtydende keramisk brændselscelle, der fungerer på butangasNår nikkelkatalysatoren i keramiske brændselsceller bruges sammen med kulbrintebrændstoffer, såsom metan, propan, og butan, det kulstof, der dannes under brændstofomdannelsen, aflejres på overfladen a -
 Sorghum:Helsekost, sødemiddel og nu, farvestof til tøjBrune tøjfarver fremstillet af sorghumskaller (øverste række) matcher nøje farverne på syntetiske farvestoffer (nederste række). Kredit:American Chemical Society Sorghum har længe været en basisfø
Sorghum:Helsekost, sødemiddel og nu, farvestof til tøjBrune tøjfarver fremstillet af sorghumskaller (øverste række) matcher nøje farverne på syntetiske farvestoffer (nederste række). Kredit:American Chemical Society Sorghum har længe været en basisfø -
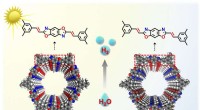 Nye isomere vinylen-bundne kovalente organiske rammer udviklet med distinkte fotokatalytiske egenska…De isomere vinylen-bundne kovalente organiske rammer. Kredit:NIMTE Forskere ledet af prof. Zahng Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) fra det kinesiske videnskab
Nye isomere vinylen-bundne kovalente organiske rammer udviklet med distinkte fotokatalytiske egenska…De isomere vinylen-bundne kovalente organiske rammer. Kredit:NIMTE Forskere ledet af prof. Zahng Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) fra det kinesiske videnskab -
 Forskere beskriver reaktionsforløbet i to-lags tynde metalfilmTynd kobber/guldfilm lavet med transmissionselektronmikroskop. Kredit:Sergey M. Zharkov et. al. / Journal of Solid State Chemistry , 2018. Et team af forskere fra Siberian Federal University (SF
Forskere beskriver reaktionsforløbet i to-lags tynde metalfilmTynd kobber/guldfilm lavet med transmissionselektronmikroskop. Kredit:Sergey M. Zharkov et. al. / Journal of Solid State Chemistry , 2018. Et team af forskere fra Siberian Federal University (SF
- Du kan se al den energi, der er afgivet sol med dine øjne sande eller falske?
- Hvilken del af atmosfæren påvirkes mest af UV -stråler?
- Hvad er stoffer, der ekstraheres fra råolie uden at blive ændret?
- Hvordan mus vælger den bedste flugtvej
- Strejkende arbejdere forsinker fransk raketopsendelse
- I hvilken højde er der ingen tyngdekraft?


