Hvad er produktet dannet ved katode og anode ved elektrolyse af forsuret vand?
elektrolyse af forsuret vand
* forsuret vand: Dette betyder, at vi tilsætter en lille mængde syre (som svovlsyre, h₂so₄) til vandet. Syren tilvejebringer flere hydrogenioner (H⁺), som er nødvendige for processen.
ved katoden (negativ elektrode):
* reduktion: Hydrogenioner (H⁺) får elektroner og reduceres til dannelse af brintgas (H₂).
* reaktion: 2H⁺ + 2E⁻ → H₂ (G)
ved anoden (positiv elektrode):
* Oxidation: Hydroxidioner (OH⁻) mister elektroner og oxideres for at danne iltgas (O₂) og vand.
* reaktion: 4OH⁻ → O₂ (G) + 2H₂O + 4E⁻
samlet reaktion:
Den samlede reaktion kombinerer katoderne og anodens reaktioner:
2H₂O (L) → 2H₂ (G) + O₂ (G)
Sammendrag:
* katode: Brintgas (H₂) produceres.
* anode: Oxygengas (O₂) produceres.
Fortæl mig, hvis du gerne vil have en mere detaljeret forklaring af processen!
Sidste artikelHvorfor pletter nogle metaller og korroderer?
Næste artikelKan vand adskilles i mindre dele med kemiske midler?
 Varme artikler
Varme artikler
-
 Honning, Jeg krympede cellekulturenVed at bruge en ny slags krympestråle, UT Austin-forskere kan ændre overfladen af en hydrogelpude i realtid, skabe riller (blå) og andre mønstre uden at forstyrre levende celler, såsom denne fibrobl
Honning, Jeg krympede cellekulturenVed at bruge en ny slags krympestråle, UT Austin-forskere kan ændre overfladen af en hydrogelpude i realtid, skabe riller (blå) og andre mønstre uden at forstyrre levende celler, såsom denne fibrobl -
 Video:Hvordan blyanter kan hjælpe os med at forstå fremtiden for alting (Alex vil have en jetpack)Kredit:The American Chemical Society Kemiverdenen har været begejstret for muligheden for buckyballs, grafen og kulstofnanorør i årtier. Men videnskaben har taget lang tid at indhente hypen. Så
Video:Hvordan blyanter kan hjælpe os med at forstå fremtiden for alting (Alex vil have en jetpack)Kredit:The American Chemical Society Kemiverdenen har været begejstret for muligheden for buckyballs, grafen og kulstofnanorør i årtier. Men videnskaben har taget lang tid at indhente hypen. Så -
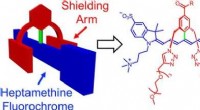 Stabile og funktionelle farvestoffer til nær-infrarød fluorescensbilleddannelse af levende individ…Kredit:Wiley Forskere kan overvåge biomolekylære processer i levende væv ved hjælp af ikke-invasive optiske metoder, såsom fluorescensbilleddannelse. Imidlertid, de fluorescerende farvestoffer, de
Stabile og funktionelle farvestoffer til nær-infrarød fluorescensbilleddannelse af levende individ…Kredit:Wiley Forskere kan overvåge biomolekylære processer i levende væv ved hjælp af ikke-invasive optiske metoder, såsom fluorescensbilleddannelse. Imidlertid, de fluorescerende farvestoffer, de -
 Selvhelende katalysatorfilm til brintproduktionForskning i retning af en mere effektiv brintproduktion:Stefan Barwe og hans kolleger. Kredit:RUB, Kramer Kemikere ved Center for Elektrokemiske Videnskaber ved Ruhr-Universität Bochum har udvikle
Selvhelende katalysatorfilm til brintproduktionForskning i retning af en mere effektiv brintproduktion:Stefan Barwe og hans kolleger. Kredit:RUB, Kramer Kemikere ved Center for Elektrokemiske Videnskaber ved Ruhr-Universität Bochum har udvikle
- Metode til at opdage mørkt stof kunne føre til en bedre forståelse af galakseudviklingen
- Vil der ske noget, hvis jorden skulle være kun 1 cm længere væk fra solen?
- Kan reaktorbrændstofrester fjernes sikkert fra Fukushima Daiichi?
- Hvordan Nantes sammenholder 3-D-print kan ændre formen på de kommende hjem
- Hvilke to ting vil øge stabiliteten i atmosfæren?
- Hawaii-vulkanen ødelægger snesevis af hjem, tvinger evakueringer


