Hvorfor er cis- og transisomerer ikke mulige for clCH2CH2CL?
Her er hvorfor:
* enkeltbindinger tillader rotation: Den enkelte binding mellem de to kulhydrater i CLCH2CH2CL er en Sigma -binding. Denne type binding tillader fri rotation omkring bindingsaksen.
* Ingen fast orientering: Rotationen betyder, at kloratomerne kan være i forskellige orienteringer i forhold til hinanden. De er ikke låst i specifikke positioner, som om de ville være i en dobbeltobligation.
Tænk på det sådan: Forestil dig en set. De to kulhydrater er omdrejningspunktet, og kloratomerne er børnene, der sidder på hver side. Useagen kan rotere frit, så børnene kan let skifte positioner. Der er ingen fast "cis" eller "trans" -konfiguration.
Kontrast med alkener:
CIS- og transisomerer * er * mulige for alkener (forbindelser med en carbon-carbon dobbeltbinding). Dette skyldes, at en dobbeltbinding består af en Sigma -obligation og en PI -obligation. PI-bindingen begrænser rotationen omkring carbon-carbonaksen og fastgør de relative placeringer af substituenter.
Fortæl mig, hvis du gerne vil have en visuel repræsentation eller have yderligere spørgsmål!
Sidste artikelEt pulver, der består af både hvide pletter og blå, vil sandsynligvis være?
Næste artikelViser 3 octene cis trans -isomerisme?
 Varme artikler
Varme artikler
-
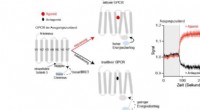 Et skridt foran inden for farmaceutisk forskningNye sensorer gør det muligt at måle aktivering eller deaktivering af GPCRer med high-throughput metoder. Kredit:Grafik:Hannes Schihada Hormoner og andre neurotransmittere, men også stoffer, virker
Et skridt foran inden for farmaceutisk forskningNye sensorer gør det muligt at måle aktivering eller deaktivering af GPCRer med high-throughput metoder. Kredit:Grafik:Hannes Schihada Hormoner og andre neurotransmittere, men også stoffer, virker -
 Forudsigelse af en regions sandsynlighed for at få fisk med toksiske niveauer af methylkviksølvKredit:Pixabay/CC0 Public Domain Indtagelse af methylkviksølv-forurenet fisk udgør en fare for menneskers sundhed. Ny forskning offentliggjort i Environmental Toxicology and Chemistry kan hjælpe em
Forudsigelse af en regions sandsynlighed for at få fisk med toksiske niveauer af methylkviksølvKredit:Pixabay/CC0 Public Domain Indtagelse af methylkviksølv-forurenet fisk udgør en fare for menneskers sundhed. Ny forskning offentliggjort i Environmental Toxicology and Chemistry kan hjælpe em -
 Vand, vand overalt - og det er mere mærkeligt, end du trorKredit:CC0 Public Domain Forskere ved University of Tokyo har brugt beregningsmetoder og analyse af nylige eksperimentelle data for at demonstrere, at vandmolekyler har to forskellige strukturer i
Vand, vand overalt - og det er mere mærkeligt, end du trorKredit:CC0 Public Domain Forskere ved University of Tokyo har brugt beregningsmetoder og analyse af nylige eksperimentelle data for at demonstrere, at vandmolekyler har to forskellige strukturer i -
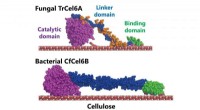 Bakteriel cellulosenedbrydningssystem kunne sætte skub i produktionen af biobrændstofferStrukturelle modeller af svampe- og bakteriecellobiohydrolaser (TrCel6A, CfCel6B) Kredit:NINS/IMS Bestræbelser på at finde måder at nedbryde cellulose - de hårde ting, der udgør plantecellevægge -
Bakteriel cellulosenedbrydningssystem kunne sætte skub i produktionen af biobrændstofferStrukturelle modeller af svampe- og bakteriecellobiohydrolaser (TrCel6A, CfCel6B) Kredit:NINS/IMS Bestræbelser på at finde måder at nedbryde cellulose - de hårde ting, der udgør plantecellevægge -
- Membraner til at opfange kuldioxid fra luften
- Hvordan en krystallinsk svamp udskiller vandmolekyler
- Hvordan bakterier kan genvinde ædle metaller fra batterier til elbiler
- Er ikke -lokalitet iboende i alle identiske partikler i universet?
- Et nyt holografisk mikroskop gør det muligt for videnskabsmænd at se gennem kraniet og afbilde mus…
- Hviskegalleritilstande i siliciumnanokegler intensiverer luminescensen


