Hvorfor er overgangsmetaller gode ledere af elektricitet?
1. Delvis fyldte d orbitaler: Overgangsmetaller har delvist fyldt D -orbitaler. Disse orbitaler er relativt tæt på energi til ledningsbåndet (båndet med energiniveau, hvor elektroner frit kan bevæge sig og udføre elektricitet).
2. Overlapning og delokalisering: D orbitaler overlapper hinanden med hinanden og med S orbitaler, der danner et bredt bånd af delokaliserede elektroner. Dette betyder, at elektronerne ikke er tæt bundet til individuelle atomer, men kan bevæge sig frit gennem metalgitteret.
3. Mobilitet af elektroner: Når et elektrisk felt påføres, kan disse delokaliserede elektroner let bevæge sig gennem metallet og bære den elektriske strøm. Denne høje elektronmobilitet bidrager til den høje ledningsevne af overgangsmetaller.
4. Metallisk binding: Den stærke metalliske binding i overgangsmetaller opstår fra delingen af disse delokaliserede elektroner. Denne stærke binding bidrager yderligere til den høje ledningsevne ved at lette elektronbevægelsen.
Kortfattet: De delvist fyldte D -orbitaler, overlappende og delokaliserede elektroner og stærk metallisk binding gør overgangsmetaller fremragende ledere af elektricitet.
Bemærk: Konduktiviteten af overgangsmetaller kan variere afhængigt af faktorer som temperatur, urenheder og det specifikke metal. Generelt betragtes de generelt som gode ledere.
 Varme artikler
Varme artikler
-
 Udnyttelse af kraften fra elektricitetsproducerende bakterier til programmerbare biohybriderKredit:CC0 Public Domain En skønne dag, mikrobielle cyborger - bakterier kombineret med elektroniske enheder - kunne være nyttige i brændselsceller, biosensorer og bioreaktorer. Men først, vidensk
Udnyttelse af kraften fra elektricitetsproducerende bakterier til programmerbare biohybriderKredit:CC0 Public Domain En skønne dag, mikrobielle cyborger - bakterier kombineret med elektroniske enheder - kunne være nyttige i brændselsceller, biosensorer og bioreaktorer. Men først, vidensk -
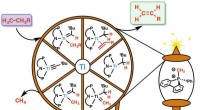 Billig, energieffektiv og ren reaktion til fremstilling af kemisk råmaterialeRepræsentation af kulstof-brint-nedbrydningsreaktionen med en spindel. Olefiner, det vil sige molekyler med en dobbeltbinding mellem kulstofatomer (C=C, grøn boks) genereres fra et ureaktivt molekyle
Billig, energieffektiv og ren reaktion til fremstilling af kemisk råmaterialeRepræsentation af kulstof-brint-nedbrydningsreaktionen med en spindel. Olefiner, det vil sige molekyler med en dobbeltbinding mellem kulstofatomer (C=C, grøn boks) genereres fra et ureaktivt molekyle -
 Solceller med nye grænsefladerKredit:CC0 Public Domain Forskere fra NUST MISIS (Rusland) og Tor Vergata-universitetet i Rom fandt ud af, at en mikroskopisk mængde todimensionalt titankarbid kaldet MXene forbedrer væsentligt op
Solceller med nye grænsefladerKredit:CC0 Public Domain Forskere fra NUST MISIS (Rusland) og Tor Vergata-universitetet i Rom fandt ud af, at en mikroskopisk mængde todimensionalt titankarbid kaldet MXene forbedrer væsentligt op -
 Sporingsmekanismer for krystallisering i realtidAlkaliske opløsninger af aluminium og natriumioner danner komplekse geler (se eksempel) sammensat af aluminiummetalcenternetværk. Under krystallisation, disse netværk frigiver ioner, hvis struktur påv
Sporingsmekanismer for krystallisering i realtidAlkaliske opløsninger af aluminium og natriumioner danner komplekse geler (se eksempel) sammensat af aluminiummetalcenternetværk. Under krystallisation, disse netværk frigiver ioner, hvis struktur påv
- Hvilken organelle fungerer i eukaryotisk cellulær respiration, hvor ATP produceres?
- Hvad er nogle eksempler på indirekte sætninger?
- Hvilket trin kommer inden man udføres i den videnskabelige metode?
- Hvordan afsky-relateret undgåelsesadfærd hjælper dyr med at overleve
- Store mængder værdifuld energi, næringsstoffer, vand tabt i verdens hurtigt stigende spildevandss…
- Forekommer solflekker på overfladen af solen?


