Hvorfor gas har en bestemt form?
Her er hvorfor:
* Partikelarrangement: Gaspartikler er meget langt fra hinanden og bevæger sig tilfældigt i alle retninger.
* svage intermolekylære kræfter: Kræfterne til tiltrækning mellem gasmolekyler er meget svage.
* høj kinetisk energi: Gaspartikler har høj kinetisk energi, hvilket betyder, at de bevæger sig hurtigt og kolliderer ofte.
På grund af disse faktorer holdes gasmolekyler ikke sammen i et fast arrangement, og de vil udvide til at udfylde enhver beholder, de er placeret i.
Tænk på det på denne måde: Forestil dig et værelse fuld af hoppekugler. Hvis du åbner døren, spreder kuglerne sig og fylder hele rummet og tager formen på rummet. Dette ligner, hvordan gas opfører sig.
væsker og faste stoffer har på den anden side bestemte former, fordi deres partikler er tættere pakket og har stærkere intermolekylære kræfter.
Sidste artikelHvordan dannes ioner af atomer?
Næste artikelHvilke ting består af atomer?
 Varme artikler
Varme artikler
-
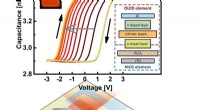 pinMOS:Ny hukommelsesenhed kan skrives på og udlæses optisk eller elektriskPinMOS-hukommelsen - en organisk halvlederenhed, der er et resultat af kombinationen af en OLED og en kondensator. Det har egenskaberne af en Memcapacitor, interagerer med lys og kan skrives og slet
pinMOS:Ny hukommelsesenhed kan skrives på og udlæses optisk eller elektriskPinMOS-hukommelsen - en organisk halvlederenhed, der er et resultat af kombinationen af en OLED og en kondensator. Det har egenskaberne af en Memcapacitor, interagerer med lys og kan skrives og slet -
 Forskning ved hjælp af atomsondetomografi afslører sprækker i jernkrystaller, der kan helesVed hjælp af jernisotoper og atomsondetomografi, eller APT, forskere skaber de første 3D atomkort over omarrangementet af forskellige jernatomer i en lille jernoxidkrystal. Kredit:PNNL Som jern, d
Forskning ved hjælp af atomsondetomografi afslører sprækker i jernkrystaller, der kan helesVed hjælp af jernisotoper og atomsondetomografi, eller APT, forskere skaber de første 3D atomkort over omarrangementet af forskellige jernatomer i en lille jernoxidkrystal. Kredit:PNNL Som jern, d -
 Proteinmolekyler i celler fungerer som miniatureantennerEn krystal af et rødt fluorescerende protein placeret i et kombineret instrument bestående af et fluorescensmikroskop og et røntgendiffraktometer. Krystallen lyser rødt, når den belyses af en blå lase
Proteinmolekyler i celler fungerer som miniatureantennerEn krystal af et rødt fluorescerende protein placeret i et kombineret instrument bestående af et fluorescensmikroskop og et røntgendiffraktometer. Krystallen lyser rødt, når den belyses af en blå lase -
 Grønne kemikere finder en måde at gøre cashewnøddeskaller til solcremeEn grafisk fremstilling af det internationale samarbejde for at finde bæredygtige løsninger til fremstilling af nyttige forbindelser. Kredit:Wits University Et team af internationale forskere har
Grønne kemikere finder en måde at gøre cashewnøddeskaller til solcremeEn grafisk fremstilling af det internationale samarbejde for at finde bæredygtige løsninger til fremstilling af nyttige forbindelser. Kredit:Wits University Et team af internationale forskere har
- Fremtiden ser lys ud for uendeligt genanvendeligt plastik
- Det virtuelle laboratorium
- Hvordan racemæssig skævhed kan begrænse internetadgang for farvede mennesker
- Navngiv to ting, der udfører mest nitrogenfiksering?
- Hvor meget naturgas er der?
- Typen af tidevand, der blev dannet i løbet af den første og tredje kvartal måne, når solen er …


