Ville svovl hexafluorid klassificeres som en ionisk forbindelse?
* ioniske forbindelser form, når et metalatom (som har en tendens til at miste elektroner) binder med et ikke -metalatom (som har en tendens til at vinde elektroner). Dette skaber en overførsel af elektroner og resulterer i modsat ladede ioner, der holdes sammen af elektrostatiske kræfter.
* svovl hexafluorid er en kovalent forbindelse . I kovalente forbindelser deler atomer elektroner for at opnå en stabil elektronkonfiguration.
Lad os nedbryde bindingen i SF₆:
* Svovl (er) er en ikke -metal.
* Fluor (F) er også en ikke -metal.
* Både svovl og fluor har en stærk tendens til at få elektroner, så de deler elektroner til dannelse af kovalente bindinger.
På grund af deling af elektroner mellem svovl og fluoratomer klassificeres svovl hexafluorid derfor som en kovalent forbindelse, ikke en ionisk forbindelse.
Sidste artikelEr denne ligning afbalanceret og i den laveste form 4NH3-2N2 6H2?
Næste artikelHvilke stoffer er de bedste isolatorer?
 Varme artikler
Varme artikler
-
 Ved at opdage genetisk materiale, hurtig sensor har potentiel anvendelse som et klinisk værktøj3D-model af DNA. Kredit:Michael Ströck/ Wikimedia/ GNU Free Documentation License På mindre end et sekund, en lille sensor, der bruges i hjernekemiforskning, kan detektere nøglemolekylerne, der gi
Ved at opdage genetisk materiale, hurtig sensor har potentiel anvendelse som et klinisk værktøj3D-model af DNA. Kredit:Michael Ströck/ Wikimedia/ GNU Free Documentation License På mindre end et sekund, en lille sensor, der bruges i hjernekemiforskning, kan detektere nøglemolekylerne, der gi -
 3D-trykt Biomesh minimerer brokreparationskomplikationer3D -printet Biomesh demonstrerer sin mekaniske styrke og fleksibilitet. Kredit:Baylor College of Medicine Brok er en af de mest almindelige bløde vævsskader. Brok dannes ved intra-abdominal indh
3D-trykt Biomesh minimerer brokreparationskomplikationer3D -printet Biomesh demonstrerer sin mekaniske styrke og fleksibilitet. Kredit:Baylor College of Medicine Brok er en af de mest almindelige bløde vævsskader. Brok dannes ved intra-abdominal indh -
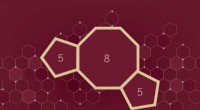 Gennembrudssyntesestrategi kan betyde bølge af nye medicinske forbindelserFSU-forskere har udtænkt en strategi til syntetisering af carbocykliske 5-8-5 smeltede ringsystemer, en molekylær struktur med potentielt bredt terapeutisk potentiale. Kredit:Benjamin Moten I farm
Gennembrudssyntesestrategi kan betyde bølge af nye medicinske forbindelserFSU-forskere har udtænkt en strategi til syntetisering af carbocykliske 5-8-5 smeltede ringsystemer, en molekylær struktur med potentielt bredt terapeutisk potentiale. Kredit:Benjamin Moten I farm -
 Forskere producerer omkostningseffektive, miljøvenligt glasmaterialeKomplekse strukturer af transparent smeltet silica fremstillet via sprøjtestøbning af den nyudviklede Glassomer-komposit. Kredit:Glassomer GmbH Glas er allestedsnærværende i højteknologiske produk
Forskere producerer omkostningseffektive, miljøvenligt glasmaterialeKomplekse strukturer af transparent smeltet silica fremstillet via sprøjtestøbning af den nyudviklede Glassomer-komposit. Kredit:Glassomer GmbH Glas er allestedsnærværende i højteknologiske produk
- Hvor kommer Amerikas gas fra?
- Et atomer af kalium har atommasse 39 amu og et tal neutroner derfor i dens nulser?
- Bob Lazar,
- Ansigtsgenkendelse udråbt som brugervenligt system til lufthavne
- Jordkulstof og nitrogenmineralisering efter den første skylning af CO2
- Hvilken sol giver lysenergi til Erth via?


