Er væske normalt tættere end gas?
* afstand af molekyler: I en væske er molekyler meget tættere sammen end i en gas. De er stadig i stand til at bevæge sig rundt (i modsætning til faste stoffer), men de er meget mere tæt pakket.
* attraktionskræfter: Kræfterne til tiltrækning mellem molekyler i en væske er stærkere end i en gas. Dette holder molekylerne tættere sammen.
Eksempel: Tænk på vand. Flydende vand er tættere end vanddamp (som er en gas). Dette er grunden til, at is flyder i vand; Is er mindre tæt end flydende vand.
Undtagelser: Der er nogle få undtagelser, normalt under ekstreme forhold:
* stærkt komprimerede gasser: Hvis en gas komprimeres til et utroligt højt tryk, kan dens densitet blive sammenlignelig med eller endda overstige en væske.
* væsker med lav densitet: Nogle væsker, som visse typer organiske opløsningsmidler, kan være mindre tætte end nogle gasser under specifikke forhold.
Men generelt er væsker tættere end gasser på grund af den tættere afstand og stærkere tiltrækning mellem deres molekyler.
 Varme artikler
Varme artikler
-
 Video:Hvad skete der præcist i Tjernobyl?Kredit:The American Chemical Society Den 26. april, 1986, Sovjetunionens atomreaktor 4 i Tjernobyl Power Complex eksploderede. Denne uge om reaktioner, vi taler om kemien bag denne katastrofale b
Video:Hvad skete der præcist i Tjernobyl?Kredit:The American Chemical Society Den 26. april, 1986, Sovjetunionens atomreaktor 4 i Tjernobyl Power Complex eksploderede. Denne uge om reaktioner, vi taler om kemien bag denne katastrofale b -
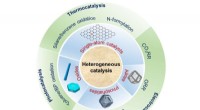 Ny anmeldelse fremhæver innovative katalysatorer:Design og anvendelseNanokatalyse spiller en afgørende rolle i den kemiske industri. Men nanokatalyse står nu over for en stor udfordring og kræver en stor revolution for at opfylde behovene i et bæredygtigt samfund. Med
Ny anmeldelse fremhæver innovative katalysatorer:Design og anvendelseNanokatalyse spiller en afgørende rolle i den kemiske industri. Men nanokatalyse står nu over for en stor udfordring og kræver en stor revolution for at opfylde behovene i et bæredygtigt samfund. Med -
 Hvordan vand hjælper substratet ind i enzymetKredit:Pixabay/CC0 Public Domain Forskere fra Bochum og Berkeley har undersøgt, hvorfor bure kan øge den katalytiske aktivitet af lukkede molekyler. Ved at bruge terahertz-spektroskopi og kompleks
Hvordan vand hjælper substratet ind i enzymetKredit:Pixabay/CC0 Public Domain Forskere fra Bochum og Berkeley har undersøgt, hvorfor bure kan øge den katalytiske aktivitet af lukkede molekyler. Ved at bruge terahertz-spektroskopi og kompleks -
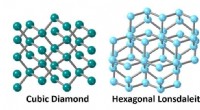 Vi skabte diamanter på få minutter uden varme ved at efterligne kraften ved en asteroide -kollisio…Krystalstrukturerne i kubisk diamant og sekskantet Lonsdaleite har atomer arrangeret forskelligt. I naturen, diamanter dannes dybt i jorden over milliarder af år. Denne proces kræver miljøer med u
Vi skabte diamanter på få minutter uden varme ved at efterligne kraften ved en asteroide -kollisio…Krystalstrukturerne i kubisk diamant og sekskantet Lonsdaleite har atomer arrangeret forskelligt. I naturen, diamanter dannes dybt i jorden over milliarder af år. Denne proces kræver miljøer med u
- Hvilke to ting har Jorden til fælles med de ydre planeter?
- Forskere finder betydelige økonomiske tab på grund af sojabønnesygdomme
- NASAs Ingenuity Mars helikopterhold siger farvel - for nu
- Hvad er den kemiske gruppe af sort onyx?
- Forskere designer superhurtig molekylær motor
- Er bor en god leder af elektricitet?


