Hvilken type opløst stof er der i en løsning, der leder elektricitet?
Her er hvorfor:
* elektrolytter er stoffer, der adskiller sig til ioner, når de opløstes i et opløsningsmiddel. Disse ioner er ladede partikler, der kan bevæge sig frit, hvilket giver løsningen til at udføre elektricitet.
* ikke -elektrolytter er stoffer, der ikke adskiller sig til ioner, når de opløstes. De forbliver som neutrale molekyler, så løsningen kan ikke udføre elektricitet.
Eksempler på elektrolytter:
* salte: Tabel salt (NaCl) opløses i Na+ og Cl- ioner.
* syrer: Hydrochlorsyre (HCI) opløses i H+ og Cl-ioner.
* baser: Natriumhydroxid (NaOH) opløses i Na+ og OH-ioner.
Eksempler på ikke -elektrolytter:
* sukker: Sucrose (C12H22O11) opløses, men danner ikke ioner.
* ethanol: Ethanol (C2H5OH) opløses, men danner ikke ioner.
Vigtig note: Styrken af den elektriske ledningsevne afhænger af koncentrationen af elektrolytten og ionens mobilitet.
Sidste artikelHvilket forhold findes mellem iltgas og luft?
Næste artikelHvad er to stoffer med lav viskositet?
 Varme artikler
Varme artikler
-
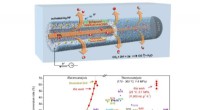 Ny sølv hulfiber booster CO2-elektroreduktionSkematisk illustration af hulfiberelektrode til at øge CO2-reduktionen til CO. Kredit:SARI Et forskerhold ledet af Profs. Wei Wei og Chen Wei fra Shanghai Advanced Research Institute (SARI) fra det
Ny sølv hulfiber booster CO2-elektroreduktionSkematisk illustration af hulfiberelektrode til at øge CO2-reduktionen til CO. Kredit:SARI Et forskerhold ledet af Profs. Wei Wei og Chen Wei fra Shanghai Advanced Research Institute (SARI) fra det -
 Fra fladskærms -tv til din smartphone - elementet bor fortjener mere opmærksomhedBor ignoreres ofte, men det har mange vigtige kvaliteter. Kredit:David Ellis/Flickr, CC BY-NC-ND Hver gang du ser sport på et fladskærms -tv, eller send en besked ved at røre ved din smartphones s
Fra fladskærms -tv til din smartphone - elementet bor fortjener mere opmærksomhedBor ignoreres ofte, men det har mange vigtige kvaliteter. Kredit:David Ellis/Flickr, CC BY-NC-ND Hver gang du ser sport på et fladskærms -tv, eller send en besked ved at røre ved din smartphones s -
 Sporing af chiralitet i realtidKunstnerens indtryk af en tidsopløst cirkulær dikroismemåling af et fotoexciteret spin-crossover-kompleks. Kredit:Ella Maru Studio, Inc. Chirale molekyler findes i to former, kaldet enantiomerer, s
Sporing af chiralitet i realtidKunstnerens indtryk af en tidsopløst cirkulær dikroismemåling af et fotoexciteret spin-crossover-kompleks. Kredit:Ella Maru Studio, Inc. Chirale molekyler findes i to former, kaldet enantiomerer, s -
 Ny teknologi kan tilbyde billigere, hurtigere mad testEn ny sikkerhedstest for fødevarebårne patogener er baseret på en ny type væskedråber, der kan binde til bakterielle proteiner. Denne interaktion, som kan detekteres med enten det blotte øje eller en
Ny teknologi kan tilbyde billigere, hurtigere mad testEn ny sikkerhedstest for fødevarebårne patogener er baseret på en ny type væskedråber, der kan binde til bakterielle proteiner. Denne interaktion, som kan detekteres med enten det blotte øje eller en
- Hvad bruger vi geotermisk energi til?
- Hvad er to måder multicellulære organismer får mad på?
- Flere af Jordens hemmeligheder skal låses op med ny krystalværktøjsforskning
- Hvilken kropsdel er i stand til tilbagetrækning?
- Carbyne-morfer, når de strækkes:Beregninger viser, at kulstof-atomkæden ville gå metal til halvl…
- En offentlig database over makromolekylære diffraktionsforsøg


