Beregn masse af klor, der kan dannes fra 50 g natriumchlorid?
1. Bestem de molære masser:
* natriumchlorid (NaCl): 22,99 g/mol (NA) + 35,45 g/mol (Cl) =58,44 g/mol
* klor (CL2): 2 * 35,45 g/mol =70,90 g/mol
2. Opret en andel:
Forholdet mellem chlormassen og massen af natriumchlorid er det samme som forholdet mellem deres molære masser.
* (Mass af Cl2 / Mass of NaCl) =(Molær masse af Cl2 / Molær masse af NaCl)
3. Løs for massen af klor (CL2):
* (masse af Cl2 / 50 g) =(70,90 g / mol / 58,44 g / mol)
* Masse af Cl2 =(70,90 g/mol * 50 g)/58,44 g/mol
* masse af Cl2 ≈ 60,6 g
Derfor kan ca. 60,6 gram klor dannes fra 50 gram natriumchlorid.
 Varme artikler
Varme artikler
-
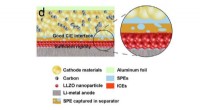 Forskere designer dendritfrit lithiumbatteriEn tynd asymmetrisk fast elektrolyt opfylder både kravene til litiummetal (blokering af dendritdannelse) og katode (muliggør lav grænseflademodstand). Kredit:H. Duan et al. ©2017 American Chemical Soc
Forskere designer dendritfrit lithiumbatteriEn tynd asymmetrisk fast elektrolyt opfylder både kravene til litiummetal (blokering af dendritdannelse) og katode (muliggør lav grænseflademodstand). Kredit:H. Duan et al. ©2017 American Chemical Soc -
 Ny hybrid 3D-printteknik vil tilføje en fjerde dimension til additiv fremstillingGrafisk abstrakt. Kredit:DOI:10.1016/j.addma.2021.102337 En ny kemisk proces til additiv fremstilling antyder spændende muligheder for 4D-printede komponenter – såsom egenskaber, der ændrer sig ov
Ny hybrid 3D-printteknik vil tilføje en fjerde dimension til additiv fremstillingGrafisk abstrakt. Kredit:DOI:10.1016/j.addma.2021.102337 En ny kemisk proces til additiv fremstilling antyder spændende muligheder for 4D-printede komponenter – såsom egenskaber, der ændrer sig ov -
 At lave masker ved hjælp af Turings matematiske modeller resulterer i effektive vandfiltreElektronmikrografer af PA-membraner af Turing-typen. (A) Lav forstørrelse SEM-billeder af de to membranoverflader. (B) SEM-billeder med høj forstørrelse af de to forskellige strukturer. (C og D) Proji
At lave masker ved hjælp af Turings matematiske modeller resulterer i effektive vandfiltreElektronmikrografer af PA-membraner af Turing-typen. (A) Lav forstørrelse SEM-billeder af de to membranoverflader. (B) SEM-billeder med høj forstørrelse af de to forskellige strukturer. (C og D) Proji -
 Ny cellulær billeddannelse baner vej for kræftbehandlingEt menneske, et enzym og nogle gelbånd - fluorescerende billeddannende midler visualiserer enzymaktivitet i sundt og sygt væv. Dette vil hjælpe med design og vurdering af mere effektive lægemidler mod
Ny cellulær billeddannelse baner vej for kræftbehandlingEt menneske, et enzym og nogle gelbånd - fluorescerende billeddannende midler visualiserer enzymaktivitet i sundt og sygt væv. Dette vil hjælpe med design og vurdering af mere effektive lægemidler mod
- Er hotspots kun form under oceanisk skorpe?
- Scholar undersøger biraciale unge politiske holdninger og selvidentifikationsfaktorer
- Hvad er stoffet i jord?
- Hvorfor er mursten ikke mineraler?
- Undersøgelse kaster mere lys over egenskaberne af en Type Ia supernova opdaget meget ung
- Forsker bruger ofte to ækvivalente temperaturenheder, graden er?


