Hvordan kan spektre fra neutrale atomer sammenlignet med spektre ioniseret af det samme element?
neutrale atomer:
* Elektronkonfiguration: Neutrale atomer har et afbalanceret antal protoner og elektroner. Dette betyder, at deres elektronkonfiguration afspejler elementets jordtilstand.
* Energiniveau: Elektronerne i neutrale atomer optager specifikke energiniveauer. Når en elektron absorberer energi, springer det til et højere energiniveau. Når det vender tilbage til et lavere niveau, udsender det en foton af lys med en bestemt energi, svarende til energiforskellen mellem niveauerne. Dette resulterer i et karakteristisk linjespektrum.
* spektrale linjer: Neutrale atomspektre udviser typisk et mere komplekst mønster af spektrale linjer, da der er mere mulige elektronovergange på grund af tilstedeværelsen af flere elektroner.
ioniserede atomer:
* Elektronkonfiguration: Ioniserede atomer har mistet en eller flere elektroner, hvilket resulterer i en positivt ladet ion. Denne ændring i antallet af elektroner ændrer elektronkonfigurationen markant.
* Energiniveau: Energiniveauet i et ioniseret atom er forskellige fra dem i det neutrale atom. Dette skyldes, at de elektrostatiske interaktioner mellem de resterende elektroner og kernen er stærkere på grund af tabet af et elektron.
* spektrale linjer: Ioniserede atomspektre er enklere end neutrale atomspektre, fordi de har færre elektroner og derfor færre mulige overgange. De spektrale linjer forskydes typisk til højere energier (kortere bølgelængder), fordi de resterende elektroner holdes mere tæt.
Nøgleforskelle:
1. Antal spektrale linjer: Neutrale atomer har generelt flere spektrale linjer end deres tilsvarende ioner.
2. Position af spektrale linjer: Ioniserede atomspektrale linjer forskydes typisk mod højere energier (kortere bølgelængder) sammenlignet med neutrale atomlinjer.
3. Intensitet af spektrale linjer: Intensiteten af spektrale linjer kan variere afhængigt af ioniseringstilstanden og den involverede specifikke overgang.
Ansøgninger:
At forstå disse forskelle er afgørende inden for forskellige områder:
* Astrofysik: Ved at analysere de spektrale linjer hos stjerner og tåge kan astronomer bestemme den kemiske sammensætning og temperaturen for disse himmelske objekter.
* Analytisk kemi: Forskere bruger emissionsspektroskopi til at identificere elementer i prøver baseret på deres unikke spektrale underskrifter.
* plasmafysik: At forstå spektre for ioniserede atomer er vigtige for at studere plasmer, som er ioniserede gasser med høj temperatur.
Kortfattet: Spektrene af neutrale og ioniserede atomer adskiller sig markant på grund af ændringer i deres elektronkonfigurationer og energiniveau. Disse forskelle har vigtige anvendelser inden for forskellige videnskabelige discipliner.
Sidste artikelHvilken gas er Pollux Star lavet af?
Næste artikelHvilken egenskab ved stof understøtter forbrænding?
 Varme artikler
Varme artikler
-
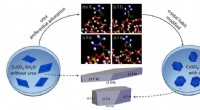 Virkningen af urinstofadditiver på krystallers fysisk -kemiske egenskaberSkematisk illustration af virkningen af urinstofadditiv på CuSO 4 · 5H 2 O krystalvane. Kredit:Prof. ZHUANGs gruppe) Krystalvaner har en betydelig indvirkning på krystallers fysisk -kemiske
Virkningen af urinstofadditiver på krystallers fysisk -kemiske egenskaberSkematisk illustration af virkningen af urinstofadditiv på CuSO 4 · 5H 2 O krystalvane. Kredit:Prof. ZHUANGs gruppe) Krystalvaner har en betydelig indvirkning på krystallers fysisk -kemiske -
 Rekonstitueret silke kan være flere gange stærkere end den naturlige fiber og fremstillet i forske…Et fotografi viser regenererede spiralformede silkefibre farvet af Rhodamine farvestoffer, under UV-lys. Kredit:Massachusetts Institute of Technology Når det kommer til at lave den komplekse bland
Rekonstitueret silke kan være flere gange stærkere end den naturlige fiber og fremstillet i forske…Et fotografi viser regenererede spiralformede silkefibre farvet af Rhodamine farvestoffer, under UV-lys. Kredit:Massachusetts Institute of Technology Når det kommer til at lave den komplekse bland -
 Verdens første bioklodser dyrket fra menneskelig urinVerdens første bio-klods lavet af menneskelig urin blev afsløret på UCT i denne uge. På billedet er (fra venstre) Department of Civil Engineering Dr. Dyllon Randall og hans studerende, Vukheta Mukhari
Verdens første bioklodser dyrket fra menneskelig urinVerdens første bio-klods lavet af menneskelig urin blev afsløret på UCT i denne uge. På billedet er (fra venstre) Department of Civil Engineering Dr. Dyllon Randall og hans studerende, Vukheta Mukhari -
 Producerer billigere, grønnere hydrogenperoxidKredit:Pixabay/CC0 Public Domain Australske forskere under ledelse af University of New South Wales har brugt Australian Synchrotron til at forstå, hvordan den kemiske struktur af et avanceret kat
Producerer billigere, grønnere hydrogenperoxidKredit:Pixabay/CC0 Public Domain Australske forskere under ledelse af University of New South Wales har brugt Australian Synchrotron til at forstå, hvordan den kemiske struktur af et avanceret kat
- Hvilke funktions danner, når floden overløb og lavt liggende land på begge sider er nedsænket i …
- Sker en måneformørkelse oftere end solformørkelse?
- Hvorfor opfandt mennesker astrologi?
- Hvorfor studerer du fårehjerner i en menneskelig anatomi -klasse?
- NASA mikrogap-køleteknologi immun over for tyngdekraftseffekter og klar til rumflyvning
- Sådan sammenlignes vaskulære og ikke-vaskulære planter


